Aktive ingredienser: Ticagrerol
Brilique 90 mg filmdrasjerte tabletter
Hvorfor brukes Brilique? Hva er den til?
Hva er Brilique
Brilique inneholder virkestoffet ticagrelor, som tilhører en gruppe legemidler som kalles trombocyttplater.
Slik fungerer Brilique
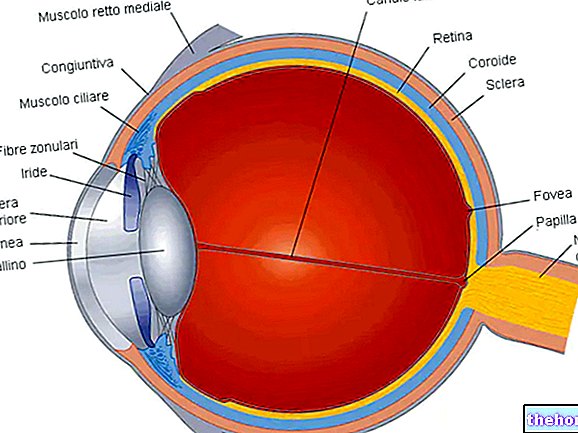
Brilique virker på celler som kalles "blodplater" (også kalt trombocytter). Disse svært små blodcellene hjelper til med å stoppe blødningen ved å klumpe seg sammen for å lukke de små hullene i avskårne eller skadede blodkar.
Imidlertid kan blodplater også danne blodpropper i de syke blodårene i hjertet og hjernen. Dette kan være svært farlig fordi:
- blodproppen kan kutte blodtilførselen helt - dette kan forårsake hjerteinfarkt (hjerteinfarkt) eller hjerneslag, eller
- blodproppen kan delvis blokkere blodårene som forsyner hjertet - dette reduserer blodstrømmen til hjertet og kan forårsake brystsmerter som kommer og går (kalt "ustabil angina"). Brilique bidrar til å blokkere blodplatene, noe som reduserer muligheten for blodpropp som kan redusere blodstrømmen.
Hva er Brilique til
Brilique i kombinasjon med acetylsalisylsyre (et annet trombocythemmende middel) skal bare brukes hos voksne pasienter.
Hun ble foreskrevet Brilique fordi hun hadde:
- et hjerteinfarkt, eller
- ustabil angina (angina eller brystsmerter som ikke er godt kontrollert).
Brilique reduserer sjansen for at du får et nytt hjerteinfarkt eller slag eller dør av hjerte- eller blodkarrelatert sykdom.
Kontraindikasjoner Når Brilique ikke skal brukes
Ikke ta Brilique hvis:
- Du er allergisk mot ticagrelor eller noen av de andre ingrediensene i Brilique
- Han har pågående blødninger
- Han fikk et hjerneslag forårsaket av blødning i hjernen.
- Du har moderate til alvorlige leverproblemer.
- Du tar en av følgende medisiner: ketokonazol (brukes til å behandle soppinfeksjoner), klaritromycin (brukes til å behandle bakterielle infeksjoner), nefazodon (et antidepressivt middel), ritonavir og atazanavir (brukes til å behandle HIV -infeksjon og AIDS)).
Ikke ta Brilique hvis noe av det ovennevnte gjelder deg. Hvis du er usikker, snakk med legen din eller apoteket før du tar Brilique
Forholdsregler for bruk Hva du må vite før du bruker Brilique
Rådfør deg med lege, apotek eller tannlege før du tar Brilique hvis:
- Du har økt risiko for blødning på grunn av:
- en alvorlig skade nylig
- en nylig operasjon (inkludert tannkirurgi)
- en sykdom som påvirker blodpropp - nylig blødning fra magesekken eller tarmen (f.eks. på grunn av magesår eller kolon "polypper")
- Du planlegger å operere (inkludert tannarbeid) når som helst mens du tar Brilique, fordi det er økt risiko for blødning. Legen din kan fortelle deg å slutte å ta Brilique 7 dager før operasjonen.
- Pulsen din er uvanlig lav (vanligvis mindre enn 60 slag per minutt), og du har ikke allerede implantert et instrument som regulerer hjerterytmen (pacemaker).
- Du har astma eller et annet lungeproblem eller pustevansker.
- Han har allerede tatt blodprøver som viste mer urinsyre enn normalt. Hvis noe av det ovennevnte gjelder deg (eller hvis du er usikker), snakk med legen din, apoteket eller tannlegen før du tar Brilique.
Barn og ungdom
Brilique anbefales ikke for barn og ungdom under 18 år.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Brilique
Fortell legen din eller apoteket dersom du bruker, nylig har brukt eller planlegger å bruke andre legemidler. Dette er fordi Brilique kan påvirke måten noen medisiner virker på, og noen medisiner kan ha effekt på Brilique.
Fortell legen din eller apoteket dersom du bruker noen av følgende medisiner:
- mer enn 40 mg simvastatin eller lovastatin daglig (legemidler som brukes til å behandle høyt kolesterol)
- rifampicin (et antibiotikum), fenytoin, karbamazepin og fenobarbital (brukes til å kontrollere anfall), digoksin (brukes til å behandle hjertesvikt), cyklosporin (brukes til å senke kroppens forsvar), kinidin og diltiazem (brukes til å behandle hjertesvikt) unormal hjerterytme ), betablokkere og verapamil (brukes til å behandle høyt blodtrykk).
Fortell spesielt legen din eller apoteket dersom du bruker noen av følgende medisiner som øker risikoen for blødning:
- "orale antikoagulantia" ofte referert til som "blodfortynnende", som inkluderer warfarin.
- ikke-steroide antiinflammatoriske legemidler (forkortet NSAIDs), ofte brukt som smertestillende midler, for eksempel ibuprofen og naproxen.
- selektive serotoninopptakshemmere (forkortet som SSRI) tatt som antidepressiva, for eksempel paroksetin, sertralin og citalopram.
- andre medisiner som ketokonazol (brukes til å behandle soppinfeksjoner), klaritromycin (brukes til å behandle bakterielle infeksjoner), nefazodon (et antidepressivt middel), ritonavir og atazanavir (brukes til å behandle HIV -infeksjon og AIDS), cisaprid (brukes mot halsbrann) eller ergot alkaloider (brukes til å behandle migrene og hodepine).
Fortell også legen din at fordi du bruker Brilique kan du ha økt risiko for blødning hvis legen din foreskriver fibrinolytika, ofte kalt 'trombolytika', for eksempel streptokinase eller alteplase.
Advarsler Det er viktig å vite at:
Graviditet og amming
Bruk av Brilique anbefales ikke hvis du er gravid eller har mistanke om graviditet. Kvinner bør bruke passende prevensjonsmetoder for å unngå å bli gravid mens de tar dette legemidlet. Snakk med legen din før du bruker Brilique hvis du ammer. Legen din vil diskutere fordeler og risiko ved behandling med Brilique med deg i løpet av denne tiden.
Rådfør deg med lege eller apotek før du bruker dette legemidlet hvis du er gravid eller ammer, tror at du kan være gravid eller planlegger å bli gravid.
Kjøring og bruk av maskiner
Det er usannsynlig at Brilique påvirker din evne til å kjøre bil eller bruke maskiner. Hvis du føler deg svimmel mens du tar Brilique, vær forsiktig når du kjører bil eller bruker maskiner
Dose, metode og administrasjonstidspunkt Hvordan bruke Brilique: Dosering
Ta alltid dette legemidlet nøyaktig slik legen din eller apoteket har fortalt deg. Rådfør deg med lege eller apotek hvis du er i tvil.
Hvor mye Brilique å ta
- Startdosen er to tabletter samtidig (180 mg ladningsdose). Denne dosen vil normalt bli gitt til deg på sykehuset.
- Etter denne startdosen er den vanlige dosen en 90 mg tablett to ganger daglig i opptil 12 måneder, med mindre legen din forteller deg noe annet. Ta Brilique på omtrent samme tid hver dag (for eksempel en tablett om morgenen og en om kvelden).
Legen din vil vanligvis fortelle deg å ta acetylsalisylsyre også. Dette er et stoff som finnes i mange medisiner som brukes for å forhindre blodpropp. Legen din vil fortelle deg hvor mye du skal ta (vanligvis mellom 75 og 150 mg per dag).
Hvordan du bruker Brilique
- Du kan ta tabletten med eller uten måltider.
- Du kan sjekke når du har tatt din siste Brilique -tablett ved å se på blisteret. Det er en sol (om morgenen) og en måne (for kvelden). Dette vil fortelle deg om du har tatt dosen.
Hvis du har problemer med å svelge tabletten (e)
Hvis du har problemer med å svelge tabletten (e), kan du knuse den og blande den med vann på følgende måte:
- Knus tabletten (e) til et fint pulver
- Hell pulveret i et halvt glass vann
- Rør og drikk umiddelbart
- For å være sikker på at du ikke har forlatt medisin, skyll det tomme glasset med et halvt glass vann og drikk.
Overdosering Hva du skal gjøre hvis du har tatt for mye Brilique
Dersom du tar for mye Brilique
Hvis du har tatt mer Brilique enn du burde, må du kontakte legen din eller gå til sykehuset med en gang. Ta medisinpakken med deg. Du kan ha økt risiko for blødning.
Dersom du har glemt å ta Brilique
- Hvis du glemmer å ta en dose, er det bare å ta neste dose som vanlig.
- Ikke ta en dobbel dose (to doser samtidig) for å gjøre opp for en glemt dose.
Hvis du slutter å ta Brilique
Ikke slutt å ta Brilique uten å snakke med legen din først. Ta Brilique regelmessig og så lenge legen din foreskriver det for deg.
Hvis du slutter å ta Brilique, kan dette øke sjansene for at du får et nytt hjerteinfarkt eller slag, eller at du dør av en sykdom relatert til hjerte- eller blodkarproblemer.
Spør lege eller apotek hvis du har ytterligere spørsmål om bruken av dette legemidlet
Bivirkninger Hva er bivirkningene av Brilique
Som alle andre legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Følgende bivirkninger kan oppstå med denne medisinen:
Se lege umiddelbart hvis du merker noen av følgende symptomer - du kan trenge akutt legehjelp:
- Blødning i hjernen eller inne i skallen er en uvanlig bivirkning og kan forårsake tegn på slag, for eksempel:
- plutselig nummenhet eller svakhet i armer, ben eller ansikt, spesielt hvis det bare er på den ene siden av kroppen
- plutselig forvirring, problemer med å snakke eller forstå andre
- plutselig vanskeligheter med å gå eller tap av balanse eller koordinering - plutselig svimmelhet eller plutselig intens hodepine uten kjent årsak
- Blødning - noen blødninger er vanlige. Imidlertid er alvorlig blødning ikke vanlig, men det kan være livstruende. Ulike typer blødninger kan økes, for eksempel:
- blødning som er alvorlig eller ikke kan kontrolleres
- uventet blødning eller blødning som varer lenge
- tilstedeværelse av blod i urinen
- produksjon av svart avføring eller rødt blod i avføringen
- synsforstyrrelser forårsaket av tilstedeværelse av blod i øynene
- frigjøring av blodpropper gjennom hoste eller oppkast
- blødning inne i leddene som resulterer i hevelse og smerte
Kontakt legen din dersom du merker noen av følgende symptomer:
- Åndepust - denne forekomsten er vanlig. Det kan skyldes hjertesykdom eller annen årsak, eller det kan være en bivirkning av Brilique. Hvis pipingen blir verre eller varer over tid, må du fortelle det til legen din. Legen din vil avgjøre om du trenger behandling eller fortsette videre undersøkelser .
Andre mulige bivirkninger
Vanlige (kan ramme opptil 1 av 10 personer)
- Blåmerker
- Neseblod
- Mer blødning fra kirurgi, kutt eller sår
Mindre vanlige (kan forekomme hos opptil 1 av 100 personer)
- Allergisk reaksjon - utslett, kløe eller hevelse i ansikt eller lepper / tunge kan være tegn på en allergisk reaksjon
- Hodepine
- Svimmelhet eller som om rommet snurrer
- Magesmerter
- Diaré eller fordøyelsesbesvær
- Følelse eller uvelhet
- Utslett
- Kløe
- Betennelse i magen (gastritt)
- Vaginal blødning som er mer intens eller oppstår på andre tidspunkter enn normal menstruasjonsblødning
- Blødning fra mageveggene (sår)
- Blødning fra tannkjøttet
Sjeldne (kan forekomme hos opptil 1 av 1000 personer)
- Forstoppelse
- Kriblende følelse
- forvirring
- Blod i ørene
- Indre blødninger
Rapportering av bivirkninger
Rådfør deg med lege eller apotek dersom du får bivirkninger, inkludert mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget. Du kan også rapportere bivirkninger direkte via det nasjonale rapporteringssystemet som er oppført i vedlegg V.
Ved å rapportere bivirkninger kan du hjelpe til med å gi mer informasjon om sikkerheten til dette legemidlet.
Utløp og oppbevaring
Ikke bruk dette legemidlet etter utløpsdatoen som er angitt på blisteren og esken etter forkortelsen EXP / EXP. Utløpsdatoen refererer til den siste dagen i den måneden. Ikke kast medisiner i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Innholdet i pakningen og annen informasjon
Hva Brilique inneholder
- Den aktive ingrediensen er ticagrelor. Hver filmdrasjerte tablett inneholder 90 mg ticagrelor.
- Andre innholdsstoffer er:
Kjernen på nettbrettet: mannitol (E421), kalsiumhydrogenfosfatdihydrat, natriumstivelsesglykolat, hydroksypropylcellulose (E463), magnesiumstearat (E470b)
Tablettbelegg: hypromellose (E464), titandioksid (E171), talkum, polyetylenglykol 400 og gult jernoksid (E172).
Beskrivelse av hvordan Brilique ser ut og innholdet i pakningen
Filmdrasjert tablett (tablett): Tablettene er runde, bikonvekse, gule, filmdrasjerte, preget med "90" over et "T" på den ene siden.
Brilique er tilgjengelig i:
- standard blister (med sol / månesymboler) i esker med 60 og 180 tabletter
- kalenderblister (med sol / månesymboler) i esker med 14, 56 og 168 tabletter
- enkeltdose perforerte blemmer i en eske med 100 x 1 tabletter.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
BRILIQUE 90 MG TABLETTER DREKKET MED FILM
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hver filmdrasjerte tablett inneholder 90 mg ticagrelor.
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Filmdrasjert tablett (tablett).
Runde, bikonvekse, gule tabletter preget med "90" over et "T" på den ene siden og slette på den andre siden.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
Brilique, administrert samtidig med acetylsalisylsyre (ASA), er indisert for forebygging av aterotrombotiske hendelser hos voksne pasienter med akutt koronarsyndrom (ustabil angina, ikke-ST segmenthøyde myokardinfarkt [NSTEMI] eller ST-segmenthøyde myokardinfarkt [STEMI] ), inkludert farmakologisk behandlede pasienter og de som gjennomgår perkutan koronar intervensjon (PCI) eller koronar bypass -podning (CABG).
For mer informasjon, se avsnitt 5.1.
04.2 Dosering og administrasjonsmåte
Dosering
Behandlingen med Brilique bør startes med en enkelt 180 mg ladningsdose (to 90 mg tabletter) og deretter fortsette med 90 mg to ganger daglig.
Pasienter som behandles med Brilique bør også ta ASA daglig, med mindre det er spesielt kontraindisert. Etter en startdose med ASA, bør Brilique tas med en vedlikeholdsdose på ASA mellom 75 og 150 mg (se pkt.5.1).
Behandling anbefales i opptil 12 måneder med mindre seponering av Brilique -behandling er klinisk indikert (se pkt.5.1) Erfaring utover 12 måneder er begrenset.
Hos pasienter med akutt koronarsyndrom (ACS) kan for tidlig seponering av noen antiplatelet -behandling, inkludert behandling med Brilique, føre til økt risiko for kardiovaskulær død eller hjerteinfarkt på grunn av pasientens underliggende sykdom. Derfor bør tidlig seponering av behandlingen unngås.
Avbrudd i kontinuitet i behandlingen bør også unngås. Pasienten som savner en dose Brilique bør bare ta en 90 mg tablett (neste dose) til planlagt tidspunkt.
Om nødvendig kan pasienter behandlet med klopidogrel byttes direkte til Brilique (se pkt.5.1). Bytte fra prasugrel til Brilique er ikke undersøkt.
Spesielle populasjoner
Pensjonister
Ingen dosejustering er nødvendig hos eldre pasienter (se pkt. 5.2).
Pasienter med nedsatt nyrefunksjon
Ingen dosejustering er nødvendig hos pasienter med nedsatt nyrefunksjon (se pkt. 5.2). Ingen informasjon er tilgjengelig om behandling av pasienter på dialyse, og derfor anbefales ikke Briliquen til disse pasientene.
Pasienter med nedsatt leverfunksjon
Brilique har ikke blitt studert hos pasienter med moderat eller alvorlig nedsatt leverfunksjon. Derfor er bruk av pasienter med moderat til alvorlig nedsatt leverfunksjon kontraindisert (se pkt. 4.3, 4.4 og 5.2). Ingen dosejustering er nødvendig hos pasienter med lett nedsatt leverfunksjon.
Pediatrisk populasjon
Sikkerhet og effekt av Brilique hos barn under 18 år for de godkjente indikasjonene hos voksne er ikke fastslått. Ingen data er tilgjengelig.
Administrasjonsmåte
For oral bruk.
Brilique kan gis til måltider eller mellom måltidene.
For pasienter som ikke klarer å svelge tabletten (e) hele, kan Brilique tabletter knuses til et fint pulver, blandes i et halvt glass vann og drikkes umiddelbart. Glasset skal skylles med et halvt glass. D "vann og innholdet drukket. Blandingen kan også administreres gjennom et nasogastrisk rør (CH8 eller større). Etter administrering av blandingen er det viktig å vanne det nasogastriske røret med vann.
04.3 Kontraindikasjoner
• Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene listet opp i pkt. 6.1 (se pkt. 4.8).
• Patologisk blødning pågår.
• Historikk om intrakranial blødning (se pkt. 4.8).
• Moderat til alvorlig nedsatt leverfunksjon (se pkt. 4.2, 4.4 og 5.2).
• Samtidig administrering av ticagrelor med sterke CYP3A4-hemmere (f.eks. Ketokonazol, klaritromycin, nefazodon, ritonavir og atazanavir) er kontraindisert, da samtidig administrering kan føre til en betydelig økning i eksponeringen av ticagrelor (se pkt. 4.5).
04.4 Spesielle advarsler og passende forholdsregler for bruk
Fare for blødning
I den sentrale fase 3 -kliniske studien (PLATO [PLATelet Inhibition and Patient Outcomes], 18 624 pasienter) inkluderte de viktigste eksklusjonskriteriene økt risiko for blødning, klinisk relevant trombocytopeni eller anemi, tidligere intrakranial blødning, gastrointestinal blødning i løpet av de foregående 6 månedene eller større operasjon de siste 30 dagene. Pasienter med akutt koronarsyndrom behandlet med Brilique og ASA viste en økt risiko for ikke-CABG-relatert større blødning og mer generelt for blødning som krevde medisinsk tilsyn, dvs. større + mindre blødninger i henhold til PLATO-kriterier, men ikke dødelige blødninger eller de som var liv -truende (se pkt. 4.8).
Derfor bør bruken av Brilique hos pasienter med kjent økt blødningsrisiko balanseres mot fordelen når det gjelder forebygging av aterotrombotiske hendelser. Hvis det er klinisk indikert, bør Brilique brukes med forsiktighet i følgende pasientgrupper:
• Pasienter med tilbøyelighet til blødning (f.eks. På grunn av nylig traume, nylig operasjon, blødningsforstyrrelser, aktiv eller nylig gastrointestinal blødning). Bruk av Brilique er kontraindisert hos pasienter med aktiv patologisk blødning, hos de som har hatt intrakraniell blødning og hos pasienter med moderat til alvorlig nedsatt leverfunksjon (se pkt. 4.3).
• Pasienter med samtidig administrering av legemidler som kan øke risikoen for blødning (f.eks. Ikke-steroide antiinflammatoriske legemidler (NSAIDs), orale antikoagulantia og / eller fibrinolytika) innen 24 timer etter dosen av Brilique.
Det er ingen data med ticagrelor om en hemostatisk fordel ved blodplatetransfusjon; den sirkulerende mengden ticagrelor kan hemme transfuserte blodplater. Siden samtidig administrering av ticagrelor og desmopressin ikke reduserte standard blødningstid, er det lite sannsynlig at desmopressin vil være effektivt i den kliniske behandlingen av blødninger (se pkt. 4.5).
Antifibrinolytisk terapi (aminokapronsyre eller tranexaminsyre) og / eller rekombinant faktor VIIa kan øke hemostase.Ticagrelor kan gjenopptas når årsaken til blødningen er identifisert og kontrollert.
Kirurgiske inngrep
Pasienter bør rådes til å informere leger og tannleger om at de tar Brilique før de planlegger en operasjon og før de tar ny medisin.
Blant PLATO -pasientene som gjennomgikk koronar bypass -transplantasjon (CABG), hadde Brilique -armen mer blødning enn klopidogrel da behandlingen ble stoppet innen 1 dag før operasjonen, men en lignende frekvens av større blødninger sammenlignet med klopidogrel da behandlingen ble stoppet 2 eller flere dager før operasjonen (se pkt. 4.8). Hvis en pasient er i ferd med å gjennomgå elektiv kirurgi og en blodplatehemmende effekt ikke er ønsket, bør Brilique seponeres 7 dager før operasjonen (se pkt.5.1).
Pasienter med risiko for bradykardi
Etter observasjoner av hovedsakelig asymptomatiske ventrikulære pauser i en tidligere klinisk studie, ble pasienter med økt risiko for bradykardi hendelser (f.eks. Pasienter uten pacemaker med sick sinus syndrom, 2. eller 3. grad AV-blokk eller bradykardirelatert synkope) ekskludert fra den sentrale PLATO studie som evaluerer sikkerhet og effekt av ticagrelor. På grunn av den begrensede kliniske erfaringen, bør ticagrelor derfor brukes med forsiktighet hos disse pasientene (se pkt. 5.1).
I tillegg bør det utvises forsiktighet ved administrering av ticagrelor samtidig med legemidler som er kjent for å indusere bradykardi. Imidlertid ble det ikke observert klinisk relevante tegn på bivirkninger i PLATO -studien etter samtidig administrering med ett eller flere legemidler som er kjent for å indusere bradykardi (f.eks. 96% betablokkere, 33% kalsiumkanalblokkere diltiazem og verapamil og 4% digoksin) ( se avsnitt 4.5).
Under undersøkelsen PLATO Holter -overvåking opplevde flere pasienter ventrikulære pauser ≥3 sekunder med ticagrelor enn med klopidogrel i den akutte fasen av ACS. Økningen i ventrikulære pauser observert på Holter med ticagrelor var større hos pasienter med kronisk hjertesvikt (CHF) enn i den totale studiepopulasjonen under den akutte fasen av ACS, men ikke etter en måned på ticagrelor eller i sammenligning med klopidogrel. Det var ingen negative kliniske konsekvenser forbundet med denne ubalansen (inkludert synkope eller pacemaker -applikasjon) i denne pasientpopulasjonen (se pkt.5.1).
Dyspné
Episoder med dyspné ble rapportert av 13,8% av pasientene som ble behandlet med Brilique og av 7,8% av pasientene som ble behandlet med klopidogrel. Hos 2,2% av pasientene anså forskerne at dyspné var årsakssammenhengende med behandling med Brilique. Dyspné er vanligvis mild til moderat i intensitet og går ofte over uten at behandlingen må avsluttes. Pasienter med astma / KOL kan ha en absolutt økt risiko for å utvikle dyspné med Brilique (se pkt. 4.8) .Ticagrelor bør brukes med forsiktighet hos pasienter med en historie astma og / eller KOLS. Mekanismen er ikke belyst. Hvis en pasient utvikler ny, langvarig eller forverret dyspné, bør dette undersøkes grundig, og hvis det ikke tolereres, bør behandlingen med Brilique avbrytes.
Forhøyelse av kreatinin
Kreatininnivået kan øke under behandling med ticagrelor (se pkt.4.8). Mekanismen er ikke avklart. Nyrefunksjonen bør overvåkes etter en måned og deretter i henhold til standard klinisk praksis, med spesiell oppmerksomhet til pasienter ≥ 75 år, til pasienter med moderat / alvorlig nedsatt nyrefunksjon og til de som får samtidig behandling med angiotensin II -antagonister.
Økt urinsyre
I PLATO -studien hadde pasienter som tok ticagrelor en høyere risiko for hyperurikemi enn de som fikk klopidogrel (se pkt. 4.8). Forsiktighet bør utvises når ticagrelor administreres til pasienter med hyperurikemi eller urinsyregikt. Som et forebyggende tiltak anbefales ikke bruk av ticagrelor hos pasienter med urinsyre -nefropati.
Annen
Basert på sammenhengen observert i PLATO-studien mellom vedlikeholdsdose av ASA og relativ effekt av ticagrelor sammenlignet med klopidogrel, anbefales ikke samtidig administrering av ticagrelor og høye vedlikeholdsdoser av ASA (> 300 mg) (se pkt.5.1).
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Ticagrelor er først og fremst et substrat for CYP3A4 og en mild hemmer av CYP3A4. Ticagrelor er også et substrat for P-glykoprotein (P-gp) og en svak hemmer av P-gp og kan øke eksponeringen for P-gp-substrater.
Effekter av andre legemidler på Brilique
Legemidler som metaboliseres av CYP3A4
CYP3A4 -hemmere
• Sterke CYP3A4-hemmere-Samtidig administrering av ketokonazol og ticagrelor økte henholdsvis 2,4 og 7,3 ganger ticagrelor Cmax og AUC. Cmax og AUC for den aktive metabolitten ble redusert med henholdsvis 89% og 56%. Andre sterke hemmere av CYP3A4 (klaritromycin, nefazodon, ritonavir og atazanavir) kan gi lignende effekter og derfor er samtidig bruk av sterke CYP3A4 -hemmere og Brilique kontraindisert (se avsnitt 4.3).
• Moderate CYP3A4-hemmere-Samtidig administrering av diltiazem og ticagrelor økte Cmax for ticagrelor med 69% og AUC med 2,7 ganger og reduserte Cmax for den aktive metabolitten med 38%, mens AUC var uendret. Det er ingen effekt av ticagrelor på plasmanivåene av diltiazem. Andre moderate CYP3A4 -hemmere (f.eks. Amprenavir, aprepitant, erytromycin og flukonazol) kan gi en lignende effekt og kan administreres sammen med Brilique.
CYP3A -indusere
Samtidig administrering av rifampicin og ticagrelor reduserte Cmax og AUC for ticagrelor med henholdsvis 73%og 86%. Cmax for den aktive metabolitten var uendret og AUC ble redusert med henholdsvis 46%. Andre CYP3A-induktorer (f.eks. Fenytoin, karbamazepin og fenobarbital) kan redusere eksponeringen for ticagrelor. Samtidig administrering av ticagrelor med potente CYP3A-induktorer kan redusere ticagrelor-eksponering og effekt, derfor anbefales det ikke samtidig bruk med Brilique.
Ciklosporin (hemmer av P-gp og CYP3A)
Samtidig administrering av cyklosporin (600 mg) og ticagrelor økte henholdsvis Cmax og AUC for ticagrelor 2,3 ganger og 2,8 ganger. AUC for den aktive metabolitten økte med 32% og Cmax reduserte. 15% i nærvær av syklosporin.
Det er ingen data om samtidig bruk av ticagrelor og andre aktive stoffer som også er potente hemmere av P-glykoprotein (P-gp) og moderate hemmere av CYP3A4 (f.eks. Verapamil, kinidin), som også kan forårsake økt eksponering for ticagrelor. Hvis denne forbindelsen ikke kan unngås, bør samtidig bruk av dem gjøres med forsiktighet.
Andre
Kliniske legemiddelinteraksjonsstudier har vist at samtidig administrering av ticagrelor med heparin, enoksaparin og ASA eller desmopressin ikke hadde noen effekt på den farmakokinetiske profilen til ticagrelor eller den aktive metabolitten eller på ADP-indusert blodplateaggregering sammenlignet med ticagrelor alene. Klinisk indikerte legemidler at alter hemostase bør brukes med forsiktighet i kombinasjon med ticagrelor.
En todelt økning i eksponering for ticagrelor har blitt observert etter daglig inntak av store mengder grapefruktjuice (3 x 200 ml) per dag. Denne størrelsen på eksponeringsøkningen antas ikke å være klinisk relevant for de fleste pasienter. .
Effekter av Brilique på andre legemidler
Legemidler som metaboliseres av CYP3A4
• Simvastatin -Samtidig administrering av ticagrelor og simvastatin økte simvastatin C med 81% og AUC med 56%, og resulterte i en økning i simvastatinsyre C med 64% og AUC med 52%, med enkelte individuelle trinn større enn 2 til 3 ganger. Samtidig administrering av ticagrelor- og simvastatindoser større enn 40 mg daglig kan forårsake bivirkninger på grunn av simvastatin, og bør avveies mot de potensielle fordelene Det var ingen effekt av simvastatin på plasmanivåene av ticagrelor. Ticagrelor kan forårsake lignende effekter på lovastatin. Samtidig bruk av ticagrelor og doser av simvastatin eller lovastatin større enn 40 mg anbefales ikke.
• Atorvastatin -Samtidig administrering av atorvastatin og ticagrelor økte Cmax for atorvastatinsyre med 23% og AUC med 36%. Lignende økninger i AUC og Cmax ble observert for alle metabolitter av atorvastatinsyre Disse økningene anses ikke som klinisk signifikante.
• En lignende effekt på andre statiner som metaboliseres av CYP3A4 kan ikke utelukkes. PLATO -pasientene som mottok ticagrelor tok en rekke statiner, uten problem med en sammenheng med statinsikkerhet hos 93% av PLATO -kohorten av pasientene som tok disse legemidlene.
Ticagrelor er en mild hemmer av CYP3A4. Samtidig administrering av ticagrelor- og CYP3A4-substrater med lave terapeutiske indekser (dvs. cisaprid eller ergotalkaloider) anbefales ikke, da ticagrelor kan øke eksponeringen for disse legemidlene.
P-glykoprotein (P-gp) substrater (inkludert digoksin, cyklosporin)
Samtidig administrering av Brilique økte digoksin Cmax med 75% og "AUC med 28%. Gjennomsnittlige" nedstrøms "digoksinnivåer ble økt med omtrent 30% ved samtidig administrering av ticagrelor, med 2 ganger maksimal individuell økning i nærvær av digoksin , Cmax og AUC for ticagrelor og dets aktive metabolitt ble ikke påvirket.
Derfor anbefales passende klinisk og / eller laboratorieovervåking ved administrering av legemidler med lav terapeutisk indeks avhengig av P-gp, for eksempel digoksin, samtidig med ticagrelor.
Det var ingen effekt av ticagrelor på blodnivået av cyklosporin.Ticagrelors effekt på andre P-gp-substrater er ikke undersøkt.
Legemidler som metaboliseres av CYP2C9
Samtidig administrering av ticagrelor og tolbutamid resulterte i ingen endring i plasmanivåene for noen av legemidlene, noe som indikerer at ticagrelor ikke er en CYP2C9 -hemmer og sannsynligvis ikke påvirker den CYP2C9 -medierte metabolismen av legemidler som warfarin og tolbutamid.
Orale prevensjonsmidler
Samtidig administrering av ticagrelor og levonorgestrel og etinyløstradiol økte eksponeringen for etinyløstradiol med omtrent 20%, men endret ikke den farmakokinetiske profilen til levonorgestrel. Det forventes ingen klinisk relevant effekt på effekten av det orale prevensjonsmiddelet etter samtidig bruk av levonorgestrel og etinylestradiol og ticagrelor.
Legemidler som er kjent for å indusere bradykardi
Etter observasjon av hovedsakelig asymptomatiske ventrikulære pauser og bradykardi, bør det utvises forsiktighet ved administrering av Brilique samtidig med andre bradykardi-induserende legemidler (se pkt. 4.4) Imidlertid ble det ikke observert tegn på klinisk bivirkninger i PLATO-studien. Signifikant etter samtidig administrering med ett eller flere legemidler som er kjent for å indusere bradykardi (f.eks. 96% betablokkere, 33% kalsiumkanalblokkere diltiazem og verapamil og 4% digoksin).
Andre samtidige behandlinger
I PLATO -studien ble Brilique vanligvis administrert sammen med ASA, protonpumpehemmere, statiner, betablokkere, angiotensinkonverterende enzymhemmere og angiotensinreseptorantagonister, som kreves av samtidige kliniske tilstander, over lang tid og også med heparin, lavmolekylære vekt heparin og kortsiktige intravenøse GpIIb / IIIa-hemmere (se pkt. 5.1) Det ble ikke observert tegn på klinisk relevante bivirkninger med disse legemidlene.
Samtidig administrering av ticagrelor og heparin, enoksaparin eller desmopressin har ingen effekt på aktivert delvis tromboplastintid (aPTT), aktivert koaguleringstid (ACT) eller faktor Xa-doser. På grunn av potensielle farmakodynamiske interaksjoner bør det utvises forsiktighet ved samtidig administrering av Brilique med legemidler som er kjent for å svekke hemostase.
Etter rapporter om unormale hudblødninger med SSRI (f.eks. Paroksetin, sertralin og citalopram) bør det utvises forsiktighet ved administrering av SSRI med ticagrelor, da dette kan føre til økt blødningsrisiko.
04.6 Graviditet og amming
Kvinner i fertil alder
Kvinner i fertil alder må ta passende prevensjonstiltak for å unngå mulig graviditet under behandling med Brilique.
Svangerskap
Det er ingen eller begrenset informasjon om bruk av ticagrelor hos gravide kvinner.
Dyrestudier har vist reproduksjonstoksisitet (se pkt. 5.3). Brilique anbefales ikke under graviditet.
Foringstid
Farmakodynamiske / toksikologiske data på dyr har vist at ticagrelor og dets aktive metabolitter skilles ut i melk (se pkt. 5.3). En risiko for nyfødte / spedbarn kan ikke utelukkes. Det må tas en beslutning om amming eller amming skal avbrytes. Avbryte / avstå fra Brilique -terapi tar hensyn til fordelen av amming for babyen og fordelen med terapi for moren.
Fruktbarhet
Ticagrelor har ingen effekt på fruktbarhet hos hann eller hunn hos dyr (se pkt. 5.3).
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Brilique har ingen eller ubetydelig påvirkning på evnen til å kjøre bil eller bruke maskiner. Svimmelhet er rapportert under behandling av akutt koronarsyndrom. Av denne grunn bør pasienter som opplever svimmelhet være forsiktige mens de kjører bil eller bruker maskiner.
04.8 Bivirkninger
Oppsummering av sikkerhetsprofilen
De vanligste rapporterte bivirkningene hos pasienter behandlet med ticagrelor var dyspné, kontusjon og epistaxis, som forekom ved en høyere forekomst enn i klopidogrelgruppen.
Tabell over bivirkninger
Sikkerheten til Brilique hos pasienter med akutt koronarsyndrom (ustabil angina, NSTEMI og STEMI) ble evaluert i den store sentrale fase 3 -studien PLATO ([PLATelet Inhibering og pasient ELLERutfall], 18 624 pasienter), som sammenlignet pasienter behandlet med Brilique (180 mg ladningsdose Brilique og vedlikeholdsdose på 90 mg to ganger daglig) og pasienter behandlet med klopidogrel (300-600 mg ladningsdose etterfulgt av 75 mg én gang daglig som vedlikehold dose), begge gitt i kombinasjon med acetylsalisylsyre (ASA) og andre standardterapier.
Følgende bivirkninger er identifisert etter studier utført med Brilique eller har blitt rapportert etter markedsføring (tabell 1).
Bivirkninger er klassifisert i henhold til frekvens og systemorganklasse. Frekvensklasser er definert i henhold til følgende konvensjoner: Svært vanlige (≥1 / 10), Vanlige (≥1 / 100,
Flere korrelerte bivirkningsterminologier har blitt gruppert i tabell e
inkludere medisinske termer som beskrevet nedenfor:
til hyperurikemi, økt urinsyre i serum
b cerebral blødning, intrakranial blødning, hemorragisk hjerneslag
c dyspné, dyspné fra anstrengelse, dyspné i ro, nattlig dyspné
d gastrointestinal blødning, rektal blødning, tarmblødning, melaena, okkult blod
og gastrointestinal sårblødning, magesårblødning, blødning i tolvfingertarmen, blødning i magesår
f subkutant hematom, kutan blødning, subkutan blødning, petechiae
g kontusjon, hematom, blåmerker, økt tendens til blåmerker, traumatisk hematom
h hematuri, blod i urinen, blødning i urinveiene
blødning på punkteringsstedet, hematom på vaskulært punkteringssted, blødning på injeksjonsstedet, blødning på punkteringsstedet, blødning på kateterstedet
# Ingen bivirkninger av hemartrose ble rapportert i ticagrelor -armen (n = 9 235) i PLATO -studien; frekvensen ble beregnet ved hjelp av den øvre grensen for 95% konfidensintervall for poengestimatet (basert på 3 / X, hvor X representerer den totale prøven, dvs. 9 235 pasienter). Dette er beregnet som 3 /9 235, som tilsvarer den "sjeldne "frekvensklasse
## Dødelige intrakranielle blødninger er rapportert etter markedsføring
Beskrivelse av utvalgte bivirkninger
Blør
De samlede resultatene av PLATO -studiens blødningshastigheter er vist i tabell 2.
Tabell 2 - Kaplan -Meier vurdering av blødningshastigheter som en funksjon av behandlingen
Definisjoner av blødningskategorier:
Dødelig / livstruende stor blødning: Klinisk tydelig med redusert hemoglobin> 50 g / l eller transfusjon ≥ 4 enheter røde blodlegemer; eller dødelig; eller intrakranial; o intraperikardial med tamponade av hjertet; eller med hypovolemisk sjokk eller alvorlig hypotensjon som krever hypertensiv behandling eller kirurgi.
Andre større blødninger: Klinisk tydelig med hemoglobinreduksjon på 30-50 g / l eller transfusjon av 2-3 enheter røde blodlegemer; ellerbetydelig deaktiverende.
Mindre blødninger: Krever medisinsk inngrep for å stoppe eller behandle blødningen.
TIMI større blødning: Klinisk tydelig med redusert hemoglobin> 50 g / l eller intrakraniell blødning.
TIMI Mindre blødning: Klinisk tydelig med 30-50 g / l reduksjon i hemoglobin.
Brilique og klopidogrel er ikke forskjellige i frekvensen av alvorlig dødelig / livstruende blødning i henhold til PLATO-kriteriene, større total blødning i henhold til PLATO-kriteriene, større blødninger i henhold til TIMI-skalaen eller mindre i henhold til TIMI-skalaen (tabell 2) . Imidlertid forekom flere PLATO kombinerte større + mindre blødninger med ticagrelor enn med klopidogrel. Få pasienter i PLATO -studien opplevde dødelig blødning: 20 (0,2%) for ticagrelor og 23 (0,3%) for klopidogrel (se pkt. 4.4).
Faktorer som alder, kjønn, vekt, rase, geografisk region, samtidig fysisk tilstand, samtidig behandling og medisinsk historie, inkludert tidligere slag eller forbigående iskemisk angrep, var ikke forutsigende for verken total eller ikke-prosedyrerelatert større blødning, definert i henhold til PLATO kriterier. Følgelig ble det ikke identifisert noen spesiell gruppe med risiko for en bestemt blødningskategori.
CABG-relatert blødning: I PLATO-studien hadde 42% av 1584 pasienter (12% av kohorten) som ble gjennomgått koronar bypass-transplantasjon (CABG) kirurgi dødelig / livstruende stor blødning i henhold til PLATO-kriteriene, uten forskjell mellom behandlingsgrupper. CABG-relatert dødelig blødning forekom hos 6 pasienter i hver behandlingsgruppe (se pkt. 4.4).
Blødning ikke relatert til CABG og blødning ikke relatert til noen prosedyre: Brilique og klopidogrel skiller seg ikke fra ikke-CABG-relaterte Major Fatal / Livstruende blødninger, definert i henhold til PLATO-kriterier, mens Total Major blødning i henhold til PLATO-kriterier, Major i henhold til TIMI-skala og Major + Mindre i henhold til TIMI-skala, var mer vanlig med ticagrelor. På samme måte, ved eliminering av prosedyrerelaterte blødninger, ble det observert flere blødninger med ticagrelor enn med klopidogrel (tabell 2). Avbrytelse av behandlingen på grunn av ikke-prosedyreblødning var mer vanlig for ticagrelor (2,9%) enn for klopidogrel (1,2%; p
Intrakranial blødning: Flere intrakranielle blødninger uten prosedyre forekom med ticagrelor (n = 27 blødninger hos 26 pasienter, 0,3%) enn med klopidogrel (n = 14 blødninger, 0,2%), inkludert 11 blødninger med ticagrelor og 1 med klopidogrel hadde dødelig utgang. Det var ingen forskjeller i total dødelig blødning.
Dyspné
Dyspné, en følelse av kortpustethet, er rapportert hos pasienter behandlet med Brilique. Dyspniske bivirkninger (EAs) (dyspné, dyspné i hvile, dyspné ved anstrengelse, paroksysmal nattlig dyspné og nattlig dyspné), når det var assosiert, ble rapportert av 13,8% av pasientene som ble behandlet med ticagrelor og av 7,8% av pasientene som ble behandlet med klopidogrel. Hos 2,2% av pasientene som tok ticagrelor og 0,6% av pasientene som ble behandlet med klopidogrel, anså forskere at dyspné var årsakssammenhengende med behandling i PLATO -studien, og noen få tilfeller var alvorlige (0,14% for ticagrelor; 0,02% for klopidogrel), (se avsnitt 4.4). De hyppigst rapporterte symptomene på dyspné var milde til moderate i intensitet, og de fleste ble rapportert som en enkelt episode kort tid etter oppstart av behandlingen.
Sammenlignet med klopidogrel kan astma / KOL-pasienter behandlet med ticagrelor ha en økt risiko for ikke-alvorlig dyspné (3,29% for ticagrelor mot 0,53% for klopidogrel) og alvorlig dyspné (0,38%). For ticagrelor mot 0,00% for klopidogrel). Absolutt sett var denne risikoen større enn den totale befolkningen i PLATO -studien. Ticagrelor bør administreres med forsiktighet til pasienter som tidligere har hatt astma og / eller KOL (se pkt. 4.4).
Omtrent 30% av alle episoder med dyspné løste seg innen 7 dager. PLATO -studien inkluderte pasienter som hadde kongestiv hjertesvikt, kronisk obstruktiv lungesykdom eller astma ved baseline; disse pasientene og eldre rapporterte mer sannsynlig episoder med dyspné. I Brilique -gruppen avbrøt 0,9% av pasientene det aktive stoffet som studeres på grunn av dyspné sammenlignet med 0,1% av pasientene som fikk klopidogrel. Den høyere forekomsten av dyspné sett med Brilique er ikke forbundet med begynnelsen eller forverringen av hjerte- eller lungesykdom (se pkt. 4.4). Brilique påvirker ikke lungefunksjonstester.
Diagnostiske tester
Forhøyelser i kreatinin: I PLATO -studien økte serumkreatininkonsentrasjonen betydelig med mer enn 30% hos 25,5% av pasientene som tok ticagrelor sammenlignet med 21,3% av pasientene som tok klopidogrel, og mer enn 50% hos pasienter som tok ticagrelor. 8,3% av pasientene på ticagrelor ticagrelor sammenlignet med 6,7% av pasientene på klopidogrel. Forhøyelser i kreatinin> 50% var mer uttalt hos pasienter over 75 år (ticagrelor 13,6% versus klopidogrel 8, 8%), hos pasienter med alvorlig nedsatt nyrefunksjon ved baseline (ticagrelor 17,8% kontra klopidogrel 12,5%) og hos pasienter på samtidig behandling med angiontensin II -reseptorantagonister (ticagrelor 11,2%kontra klopidogrel 7, 1%). Innenfor disse undergruppene var alvorlige nyrebivirkninger og bivirkninger som førte til seponering av legemiddel lik i de to behandlingsgruppene. Totalt sett rapporterte bivirkninger i nyrene var 4,9% for ticagrelor mot 3,8% for klopidogrel, men en lignende prosentandel av pasientene rapporterte hendelser som av forskere ble ansett som direkte årsak til behandling: 54 (0,6%) for ticagrelor og 43 (0,5%) for klopidogrel.
Urinsyreforhøyelser: I PLATO -studien økte serumkonsentrasjonen av urinsyre over normalgrensen hos 22% av pasientene som ble behandlet med ticagrelor sammenlignet med 13% av pasientene som tok klopidogrel. Den gjennomsnittlige serumurinsyre -konsentrasjonen ble økt med omtrent 15% med ticagrelor sammenlignet med 7,5% med klopidogrel og redusert til omtrent 7% med ticagrelor etter seponering av behandlingen, mens ingen reduksjon ble observert med klopidogrel. Hyperurikemi-bivirkningen ble rapportert hos 0,5% for ticagrelor mot 0,2% for klopidogrel. Av disse bivirkningene ble 0,05% for ticagrelor versus 0,02% for klopidogrel ansett å være relatert til utreder-rettet årsakssammenheng. 0,2% for ticagrelor kontra 0,1% for klopidogrel; ingen av disse bivirkningene ble ansett som årsakssammenheng med behandling av etterforskerne.
Rapportering av mistenkte bivirkninger
Rapportering av mistenkte bivirkninger som oppstår etter godkjenning av legemidlet er viktig ettersom det muliggjør kontinuerlig overvåking av nytte / risiko -balansen for legemidlet Helsepersonell bes rapportere alle mistenkte bivirkninger via det nasjonale rapporteringssystemet. "Adresse" www .agenziafarmaco.gov.it/it/responsabili ".
04.9 Overdosering
Ticagrelor tolereres godt i enkeltdoser på opptil 900 mg. Gastrointestinal toksisitet var dosebegrensende i en eskaleringsstudie med enkeltdoser. Andre klinisk relevante bivirkninger som kan oppstå etter overdose inkluderer dyspné og ventrikulære pauser (se pkt. 4.8).
Ved overdosering kan de ovennevnte potensielle bivirkningene forekomme, og EKG -overvåking bør vurderes.
Til dags dato er det ingen kjent motgift for å motvirke effekten av ticagrelor, og det antas at ticagrelor ikke er dialyserbart (se pkt. 4.4). Behandling av overdosering bør følge standardene for lokal medisinsk praksis. Den forventede effekten av for mye Brilique er forlengelse av blødningsrisikoen forbundet med trombocytthemming.Hvis blødning forekommer, bør det iverksettes passende støttende medisinske tiltak.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: antiplatelet midler, unntatt heparin.
ATC -kode: B01AC24.
Virkningsmekanismen
Brilique inneholder ticagrelor, som tilhører den kjemiske klassen av cyklopentyltriazolopyrimidiner
(CPTP), som er en oral, direkte, selektiv og reversibel P2Y12 -reseptorantagonist og forhindrer adenosindifosfat (ADP) - mediert P2Y12 -avhengig blodplateaktivering og aggregering.
Ticagrelor forhindrer ikke ADP-binding, men når den binder seg til P2Y12-reseptoren forhindrer den ADP-indusert signaltransduksjon. Siden blodplater spiller en rolle i utbruddet og / eller utviklingen av trombotiske komplikasjoner av aterosklerotisk sykdom, har inhibering av blodplatefunksjon vist seg å redusere risikoen for kardiovaskulære hendelser som død, hjerteinfarkt eller hjerneslag.
Ticagrelor øker også lokale endogene nivåer av adenosin gjennom inhibering av ekvilibrativ nukleosidtransportør -1 (ENT -1).
Ticagrelor har vist seg å øke følgende adenosininduserte effekter hos friske individer og hos pasienter med ACS: vasodilatasjon (målt som økt koronar blodstrøm hos friske frivillige og hos ACS-pasienter; hodepine), inhibering av blodplatefunksjon (i fullblod) in vitro) og dyspné. Koblingen mellom den observerte økningen i adenosin og kliniske utfall (f.eks. Sykelighet-dødelighet) er imidlertid ikke klarlagt.
Farmakodynamiske effekter
Handlingens begynnelse (start)
Hos pasienter med stabil koronarsykdom behandlet med ASA, induserer ticagrelor en rask utbrudd av farmakologisk effekt, som demonstrert av en gjennomsnittlig "trombocyttaggregasjonshemming (PAH) for ticagrelor, 0,5 timer etter en 180 mg ladningsdose. Ca. 41% med en maksimal effekt på PAH på 89% innen 2-4 timer etter dose, og opprettholdt mellom 2 og 8 timer. 90% av pasientene hadde siste PAH> 70% innen 2 timer etter dose.
Handlingens reversibilitet (forskyvning)
Hvis en CABG -prosedyre var planlagt, øker risikoen for blødning med ticagrelor sammenlignet med klopidogrel når den stoppes mindre enn 96 timer før operasjonen.
Data knyttet til endring av terapi
Bytte fra klopidogrel til ticagrelor resulterer i en absolutt økning i PAH på 26,4%, mens bytte fra ticagrelor til klopidogrel resulterer i en absolutt reduksjon i PAH på 24,5%. Pasienter kan byttes fra klopidogrel til ticagrelor -behandling uten å avbryte den trombocytblodige effekten (se pkt.4.2).
Klinisk effekt og sikkerhet
PLATO-studien inkluderte 18.624 pasienter som presenterte innen 24 timer etter at symptomene på ustabil angina (UA), ikke-ST-segment forhøyet hjerteinfarkt (NSTEMI) eller ST-segment forhøyet hjerteinfarkt (STEMI) hadde oppstått, og som først hadde blitt behandlet farmakologisk med enten perkutan koronar intervensjon (PCI) eller koronar bypass -podning (CABG) (se avsnitt 4.1).
Ved den samme daglige dosen av ASA var ticagrelor 90 mg to ganger daglig bedre enn 75 mg klopidogrel daglig for å forhindre det sammensatte endepunktet for kardiovaskulær død [CV], hjerteinfarkt [MI] eller hjerneslag, med forskjellen styrt av reduksjonen av CV- og MI -dødsfall Pasientene mottok enten en 300 mg ladningsdose klopidogrel (600 mg dose mulig for PCI) eller 180 mg ticagrelor.
Resultatet ble oppnådd tidlig (absolutt risikoreduksjon [ARR] 0,6% og relativ risikoreduksjon [RRR] med 12% etter 30 dager), med en behandlingseffekt som forble konstant over 12 måneder, og oppnådde en "ARR" på 1,9% per år og en RRR på 16%. Disse dataene tyder på at det er hensiktsmessig å behandle pasienter med ticagrelor i opptil 12 måneder (se pkt. 4.2). Behandling av 54 ACS -pasienter med ticagrelor i stedet for at det med klopidogrel ville unngå utbrudd av 1 aterotrombotisk hendelse ; behandling av 91 pasienter ville unngå 1 CV -død (tabell 3).
Effekten av ticagrelorbehandling sammenlignet med klopidogrel er konsistent for alle undergrupper av pasienter etter egenskaper, inkludert vekt, kjønn, diabetes mellitus, forbigående iskemisk anfall eller ikke-hemoragisk slag, revaskularisering, samtidig behandling inkludert hepariner, GpIIb / IIIa-hemmere og protonpumpe hemmere (se pkt. 4.5), endelig diagnose av hendelsen (STEMI, NSTEMI eller UA) og behandlingsvei tildelt randomisering (invasiv eller medisinsk).
En svakt signifikant interaksjon ble observert mellom behandling og geografisk region, der Hazard Ratio (HR) for det primære endepunktet favoriserer ticagrelor i resten av verden, mens det favoriserer klopidogrel i Nord -Amerika, som utgjør omtrent 10%av det globale. populasjonsstudier (p-verdi av interaksjonen = 0,045).
Utforskende analyser antyder en mulig sammenheng med ASA -dose, siden redusert effekt ble observert med ticagrelor assosiert med økende doser ASA Den daglige kroniske dosen av ASA, gitt sammen med Brilique, bør være mellom 75 og 150 mg (se pkt. 4.2 og 4.4) .
Figur 1 viser den estimerte risikoen for første forekomst av enhver hendelse vurdert i det sammensatte effektpunktet.
Brilique reduserte starten på det primære sammensatte endepunktet sammenlignet med klopidogrel i både UA / NSTEMI- og STEMI -populasjonene (tabell 3).
Tabell 3 - Kliniske utfall i PLATO -studien
a ARR = absolutt risikoreduksjon; RRR = relativ risikoreduksjon = (1-Hazard ratio) x 100%. En negativ RRR indikerer en økt relativ risiko.
b ekskludert stille hjerteinfarkt.
c SRI = alvorlig tilbakevendende iskemi; RI = tilbakevendende iskemi; TIA = forbigående iskemisk angrep; ATE = aterotrombotisk hendelse. Total MI inkluderer stille MI, med hendelsesdato angitt som diagnosedato.
d verdi av nominell betydning; alle andre verdier er formelt statistisk signifikante basert på en forhåndsdefinert hierarkisk test.
Holter delstudie
For å studere begynnelsen av ventrikulære pauser og andre arytmiske episoder under PLATO -studien, utførte etterforskerne Holter -overvåking i en undergruppe på nesten 3000 pasienter, hvorav omtrent 2000 hadde poster knyttet til både den akutte fasen av koronarsyndrom. Akutt, enten etter en måned. Den primære variabelen av interesse var starten på ventrikulære pauser ≥3 sekunder. Flere pasienter opplevde ventrikulære pauser med ticagrelor (6,0%) enn med klopidogrel (3,5%) i den akutte fasen; henholdsvis 2,2% og 1,6% etter 1 måned (se pkt. 4.4). Økningen i ventrikulære pauser i den akutte fasen av ACS var mer uttalt hos tikagrelorbehandlede pasienter med en historie med CHF (9,2% mot 5,4% hos pasienter uten en historie med CHF; for klopidogrelbehandlede pasienter, 4,0% hos pasienter med en historie med CHF mot 3,6% hos de uten en historie med CHF). Denne forskjellen ble ikke observert etter en måned: 2,0% versus 2,1% for ticagrelorbehandlede pasienter med henholdsvis og uten CHF; og 3,8% mot 1,4% med klopidogrel.Ingen negative kliniske konsekvenser forbundet med denne forskjellen (inkludert pacemaker -applikasjoner) ble funnet i denne pasientpopulasjonen.
Genetikkundersøkelse fra PLATO -studien
Genotyping av CYP2C19 og ABCB1 av 10 285 pasienter fra PLATO -studien tillot å knytte de kliniske resultatene av studien til den genotypiske fordelingen. Ticagrelors overlegenhet over klopidogrel for å redusere store kardiovaskulære hendelser ble ikke påvirket av pasientens CYP2C19- eller ABCB1 -genotype. I likhet med de generelle dataene fra PLATO -studien, var forekomsten av total større blødninger etter PLATO -kriterier ikke forskjellig mellom ticagrelor og klopidogrel, uansett av CYP2C19- eller ABCB1 -genotypen. Forekomsten av PLATO Non-CABG-relaterte større blødninger ble økt med ticagrelor sammenlignet med klopidogrel hos pasienter med en eller flere CYP2C19-funksjonsalleler, men lik klopidogrel hos pasienter uten reduserte funksjonsalleler.
Sammensatt sammenslutning av effekt og sikkerhet
Den sammensatte kombinasjonen av effekt og sikkerhet (CV -død, MI, hjerneslag eller PLATO Total større blødning) indikerer at effektfordelen med Brilique fremfor klopidogrel ikke blir negert av større blødninger (ARR 1, 4%; RRR 8%; HR 0,92 ; p = 0,0257) i de 12 månedene etter SCA.
Pediatrisk populasjon
Det europeiske legemiddelkontoret har frafalt forpliktelsen til å levere resultatene av studier med Brilique i alle undergrupper av den pediatriske populasjonen i den godkjente indikasjonen (se pkt. 4.2 og 5.2).
05.2 Farmakokinetiske egenskaper
Ticagrelor viser lineær farmakokinetikk og eksponering for ticagrelor og den aktive metabolitten (AR-C124910XX) er tilnærmet dose proporsjonale opptil 1260 mg.
Absorpsjon
Absorpsjonen av ticagrelor er rask, med en gjennomsnittlig t på omtrent 1,5 time. Dannelsen av hovedmetabolitten i sirkulasjon, AR-C124910XX (også aktiv), avledet fra ticagrelor, er rask, med en t
median på ca 2,5 timer. Etter oral administrering av 90 mg ticagrelor under faste, er Cmax 529 ng / ml og AUC er 3 451 ng xh / ml Forløpermetabolittforholdet er 0,28 for Cmax og 0,42 for AUC.
Gjennomsnittlig absolutt biotilgjengelighet for ticagrelor ble estimert til å være 36%. Inntak av et fettrikt måltid forårsaket en 21% økning i AUC for ticagrelor og en 22% reduksjon i Cmax for den aktive metabolitten, men hadde ingen effekt på Cmax for ticagrelor eller AUC for ticagrelor. Aktiv metabolitt. Disse små endringer anses å ha minimal klinisk relevans, derfor kan ticagrelor administreres både med og fra måltider. Ticagrelor og dets aktive metabolitt er substrater for P-gp.
Ticagrelor som knuste tabletter blandet i vann, administrert oralt eller gjennom et nasogastrisk rør i magen, har en sammenlignbar biotilgjengelighet for hele tabletter for AUC og Cmax for både ticagrelor og den aktive metabolitten. Initial eksponering (0, 5 og 1 time etter dose) for knuste ticagrelor -tabletter blandet i vann var høyere enn for hele tabletter, med en konsentrasjonsprofil fra da av generelt identisk (2 til 48 timer).
Fordeling
Distribusjonsvolumet for ticagrelor i steady state er 87,5 L. Ticagrelor og dets aktive metabolitt er i stor grad bundet til plasmaproteiner (> 99,0%).
Biotransformasjon
CYP3A4 er det viktigste enzymet som er ansvarlig for metabolismen av ticagrelor og dannelsen av den aktive metabolitten, og deres interaksjoner med andre CYP3A -substrater spenner fra aktivering til inhibering.
Hovedmetabolitten til ticagrelor er AR-C124910XX, som også har farmakologisk aktivitet, som vist in vitro ved binding til blodplate P2Y12-reseptoren til ADP Systemisk eksponering for den aktive metabolitten er omtrent 30-40% av den som ble observert med ticagrelor.
Eliminering
Den primære ruten for eliminering av ticagrelor er via hepatisk metabolisme. Når radiomerket ticagrelor administreres, er gjennomsnittlig gjenoppretting av radioaktivitet omtrent 84% (57,8% i avføring, 26,5% i urin). De gjenopprettede mengdene av både ticagrelor og den aktive metabolitten, som er tilstede i urinen, var mindre enn 1% av dose.
Den primære elimineringsveien for den aktive metabolitten er sannsynligvis gallsekresjon. Gjennomsnittlig t1 / 2 var omtrent 7 timer for ticagrelor og 8,5 timer for den aktive metabolitten.
Spesielle populasjoner
Pensjonister
Høyere eksponering for ticagrelor (ca. 25% for både Cmax og AUC) og den aktive metabolitten ble observert hos eldre pasienter (≥75 år) med ACS sammenlignet med yngre pasienter, via en "populasjonsfarmakokinetisk analyse. Anses som klinisk signifikant (se pkt.4.2 ).
Pediatrisk populasjon
Ticagrelor er ikke evaluert i den pediatriske populasjonen (se pkt. 4.2 og 5.1).
Kjønn
Høyere eksponering av ticagrelor og den aktive metabolitten ble observert hos kvinner enn hos menn. Disse forskjellene anses ikke som klinisk signifikante.
Nedsatt nyrefunksjon
Eksponeringen for ticagrelor var omtrent 20% lavere og aktiv metabolitteksponering var omtrent 17% høyere hos pasienter med alvorlig nedsatt nyrefunksjon (kreatininclearance
Nedsatt leverfunksjon
Cmax og AUC for ticagrelor var 12% og 23% høyere hos pasienter med lett nedsatt leverfunksjon sammenlignet med et sammenlignbart utvalg av friske personer (se pkt.4.2). Ticagrelor er ikke undersøkt hos pasienter med moderat eller alvorlig nedsatt leverfunksjon, og bruk hos disse pasientene er kontraindisert (se pkt. 4.3 og 4.4).
Etnisitet
Pasienter med asiatisk avstamning viser en gjennomsnittlig biotilgjengelighet som er 39% høyere enn kaukasiske pasienter. Pasienter som ble identifisert som svarte, hadde en 18% lavere biotilgjengelighet av ticagrelor enn kaukasiske pasienter. I kliniske farmakologiske studier var eksponeringen (Cmax og AUC) for ticagrelor hos japanske pasienter omtrent 40% (20% etter justering for kroppsvekt) høyere enn hos kaukasiske pasienter.
05.3 Prekliniske sikkerhetsdata
Prekliniske data for ticagrelor og dets viktigste metabolitt viste ikke en uakseptabel risiko for bivirkninger for mennesker basert på konvensjonelle studier av sikkerhetsfarmakologi, toksisitet ved én eller gjentatt dosering og gentoksisk potensial.
Gastrointestinal irritasjon ble observert hos flere dyrearter for klinisk relevante eksponeringsnivåer (se pkt. 4.8).
Hos hunnrotter viste ticagrelor ved høye doser økt forekomst av livmorsvulster (adenokarsinomer) og økt forekomst av hepatiske adenomer. Mekanismen for utbrudd av livmorsvulster er sannsynligvis relatert til en hormonell ubalanse som kan føre til svulstdannelse hos rotter. Mekanismen som ligger til grunn for dannelsen av hepatiske adenomer skyldes sannsynligvis en gnagerspesifikk hepatisk enzyminduksjon. Derfor anses observasjonene knyttet til det kreftfremkallende potensialet å være av usannsynlig relevans for mennesker.
Mindre utviklingsforstyrrelser ble observert hos rotter ved en maternelt toksisk dose (sikkerhetsmargin 5.1). Hos kaniner ble det observert en liten forsinkelse i levermodenhet og skjelettutvikling hos fostre fra mødre som ble utsatt for høye doser, uten tegn på mors toksisitet (sikkerhetsmargin 4,5).
Studier på rotter og kaniner har vist reproduksjonstoksisitet, med liten nedgang i mors kroppsvektøkning, redusert levedyktighet hos nyfødte og reduksjon i fødselsvekt, med veksthemming.Ticagrelor forårsaket uregelmessige sykluser (hovedsakelig lengre sykluser) hos hunnrotter, men forårsaket ikke effekter generell fruktbarhet hos hann- og hunnrotter Farmakokinetiske studier utført med radiomerket ticagrelor viste at moderforbindelsen og dens metabolitter skilles ut i melk hos rotter (se pkt. 4.6).
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Kjernen på nettbrettet
Mannitol (E421)
Kalsiumhydrogenfosfatdihydrat
Magnesiumstearat (E470b)
Natriumstivelsesglykolat
Hydroksypropylcellulose (E463)
Tablettbelegg
Talkum
Titandioksid (E171)
Gult jernoksid (E172)
Polyetylenglykol 400
Hypromellose (E464)
06.2 Uforlikelighet
Ikke relevant.
06.3 Gyldighetsperiode
3 år.
06.4 Spesielle forholdsregler for lagring
Dette legemidlet krever ingen spesielle oppbevaringsbetingelser.
06.5 Emballasje og innhold i pakningen
• Gjennomsiktig blister (med sol / månesymboler) i PVC-PVDC / Al på 10 tabletter; esker med 60 tabletter (6 blister) og 180 tabletter (18 blister).
• Gjennomsiktig kalenderblister (med sol / månesymboler) i PVC-PVDC / Al på 14 tabletter; esker med 14 tabletter (1 blister), 56 tabletter (4 blister) og 168 tabletter (12 blister).
• Gjennomsiktig enkeltdose perforert blister i PVC-PVDC / Al på 10 tabletter; esker med 100 x 1 tabletter (10 blister).
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering
Ingen spesielle instruksjoner.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
AstraZeneca AB
SE-151 85
Södertälje
Sverige
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
EU / 1/10/655 / 001-006
040546018
040546020
040546032
040546044
040546057
040546069
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
Dato for første godkjenning: 3. desember 2010
Dato for siste fornyelse: 17. juli 2015
10.0 DATO FOR REVISJON AV TEKSTEN
Juli 2015