Hva er Nymusa?
Nymusa er en infusjonsvæske, oppløsning (drypp i en vene) som inneholder virkestoffet koffeinsitrat (20 mg / ml). Løsningen kan også tas oralt.
Hva brukes Nymusa til?
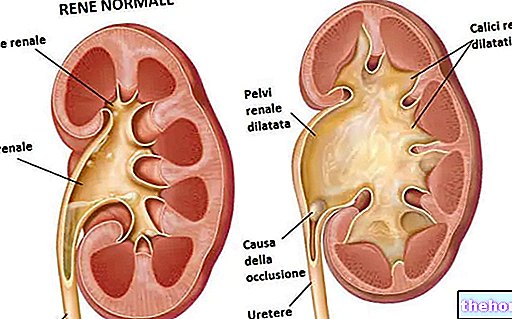
Nymusa brukes til behandling av primær apné hos premature spedbarn. Hos spedbarnet er apné opphør av å puste i mer enn 20 sekunder; Med "primær" menes det faktum at den ikke har noen åpenbar årsak. Medisinen kan bare fås på resept.
Fordi antallet premature babyer med primær apné er lavt, blir sykdommen betraktet som 'sjelden', og Nymusa ble betegnet som 'foreldreløs medisin' (et legemiddel som brukes i sjeldne sykdommer) 17. februar 2003.
Hvordan brukes Nymusa?
Behandling med Nymusa bør bare startes under tilsyn av en lege som har erfaring med behandling av spedbarn som trenger intensivbehandling. Behandling med stoffet bør bare utføres på en nyfødt intensivavdeling som er egnet for overvåking av babyen.
Behandlingen starter med en dose på 20 mg per kilo kroppsvekt, som skal gis samtidig med langsom infusjon som varer i 30 minutter. Etter 24 timer er det mulig å starte daglig administrering av en vedlikeholdsdose på 5 mg per kg kroppsvekt, ved langsom infusjon som varer i 10 minutter eller gjennom munnen gjennom et nasogastrisk rør (et rør som settes inn i nesen og når magen )..
Om nødvendig kan legen overvåke blodnivået av koffein i babyen, muligens korrigere dosen. Legen din slutter å ta Nymusa når fem til syv påfølgende dager har gått uten apné.
Hvordan fungerer Nymusa?
Hos premature babyer skyldes apné en ufullstendig utvikling av hjernesentrene som er ansvarlige for å puste.Den aktive ingrediensen i Nymusa, koffeinsitrat, er en stimulant for nervesystemet.Koffeinsitrat er en "antagonist" av adenosin, et stoff som blokkerer aktiviteten til noen deler av hjernen, inkludert den som styrer pusten. Ved apné virker koffeinsitrat ved å blokkere reseptorene som adenosin normalt binder seg til, og reduserer dermed effekten av adenosin og stimulerer hjernen til å reaktivere pusten.
Hvordan har Nymusa blitt studert?
Siden koffeinsitrat har blitt brukt i lang tid hos premature babyer, presenterte selskapet data fra vitenskapelig litteratur. I en publisert studie som involverte 85 premature babyer med flere apné -episoder, ble koffeinsitrat sammenlignet med placebo (en dummy -behandling). Hovedmålet for effektivitet var basert på å redusere det daglige antallet apnéepisoder til minst halvparten i løpet av ti dager.
En stor publisert studie sammenlignet koffeinsitrat med placebo ved behandling av premature babyer med apné i 2006. Studien så på hvor lenge barna overlevde og om de hadde nevrologiske handikap eller ikke etter 18 måneder.
I en publisert gjennomgang av fem studier ble koffein og teofyllin (et annet stimulant) sammenlignet med placebo hos 192 premature babyer med apné. Hovedmål for effektivitet var antall pasienter uten "terapeutisk svikt", forstått som mangel på halvering av apneiske episoder, eller behovet for å ty til assistert pust eller barnets død.
Hvilken fordel har Nymusa vist under studiene?
Koffeinsitrat var mer effektivt enn placebo ved behandling av apné hos premature spedbarn. På 6 av 10 dager var koffeinsitrat mer effektivt enn placebo for å redusere antallet apnéepisoder med minst halvparten. Antall spedbarn behandlet med koffeinsitrat og som tilbrakte minst åtte dager uten apneiske episoder, 22% av spedbarn behandlet med koffeinsitrat sammenlignet med ingen spedbarn behandlet med placebo.
I en stor publisert studie døde 46% av spedbarn som ble behandlet med placebo (431 av 932) eller rapporterte nevrologiske handikap, sammenlignet med 40% av spedbarn behandlet med koffeinsitrat (377 av 937).
I gjennomgangen av de fem studiene var det færre behandlingssvikt hos barn behandlet med koffein eller teofyllin enn hos de som ble behandlet med placebo.
Hva er risikoen forbundet med Nymusa?
De vanligste bivirkningene forbundet med koffeinsitrat (dvs. sett hos 1 til 10 pasienter av 100) er flebitt (betennelse i en vene) på infusjonsstedet og betennelse på infusjonsstedet. Den fullstendige listen over bivirkninger rapportert med koffeinsitrat, se pakningsvedlegget.
Nymusa skal ikke brukes til babyer som kan være overfølsomme (allergiske) overfor koffeinsitrat eller noen av de andre ingrediensene.
Hvorfor har Nymusa blitt godkjent?
Komiteen for medisiner for mennesker (CHMP) bestemte at fordelene ved Nymusa er større enn risikoen ved behandling av primær apné hos premature spedbarn, og anbefalte at Nymusa ble gitt markedsføringstillatelse.
Hvilke tiltak iverksettes for å sikre sikker bruk av Nymusa?
Selskapet som produserer Nymusa har forpliktet seg til å utarbeide et kort som skal legges ut på intensivavdelingene der legemidlet skal brukes, etter avtale med medlemsstatene. dette arket vil inneholde informasjon om hvordan Nymusa administreres, doseringene, behovet for å overvåke nivåene av koffein i plasma og de uønskede effektene som kan oppstå under
behandling.
Annen informasjon om Nymusa:
Juli 2009 ga EU -kommisjonen Chiesi Farmaceutical SpA en "markedsføringstillatelse" for Nymusa, gyldig i hele EU.
For sammendrag av uttalelsen fra Committee for Orphan Medicinal Products for Nymusa, klikk her.
For hele versjonen av Nymusas EPAR, klikk her.
Siste oppdatering av dette sammendraget: 05-2009.
Informasjonen om Nymusa - koffeinsitrat publisert på denne siden kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.











-cos-cause-e-terapia.jpg)