Aktive ingredienser: Paliperidon
XEPLION 25 mg injeksjonsvæske, suspensjon
XEPLION 50 mg injeksjonsvæske, suspensjon
XEPLION 75 mg injeksjonsvæske, suspensjon
XEPLION 100 mg injeksjonsvæske, suspensjon
XEPLION 150 mg injeksjonsvæske, suspensjon
Indikasjoner Hvorfor brukes Xeplion? Hva er den til?
Xeplion inneholder virkestoffet paliperidon, som tilhører klassen antipsykotiske medisiner og brukes som vedlikeholdsbehandling for symptomer på schizofreni hos voksne pasienter stabilisert på paliperidon eller risperidon.
Hvis du tidligere har vist å svare på paliperidon eller risperidon og har milde til moderate symptomer, kan legen din starte behandling med Xeplion uten tidligere stabilisering med paliperidon eller risperidon.
Schizofreni er en sykdom preget av "positive" og "negative" symptomer. Positiv betyr et overskudd av symptomer som normalt ikke er tilstede. For eksempel kan en person med schizofreni høre stemmer eller se ting som ikke faktisk eksisterer (kalt hallusinasjoner), tro på ting som ikke er sanne (kalt vrangforestillinger), eller være uvanlig mistenksom overfor andre. Negative symptomer betyr mangel på atferd eller følelser som normalt er tilstede. For eksempel kan en person med schizofreni ha en tendens til å være isolert og ikke reagere følelsesmessig eller kan ha problemer med å snakke klart og logisk. Personer med denne lidelsen kan også føle seg deprimert, engstelig, skyldig eller anspent.
Xeplion kan bidra til å lindre symptomene på sykdommen din og forhindre at de kommer tilbake.
Kontraindikasjoner Når Xeplion ikke skal brukes
Ikke bruk Xeplion
- dersom du er allergisk mot paliperidon eller noen av de andre innholdsstoffene i dette legemidlet (listet opp i avsnitt 6).
- hvis du er allergisk mot et annet antipsykotisk legemiddel, inkludert risperidon.
Forholdsregler for bruk Hva du trenger å vite før du bruker Xeplion
Snakk med legen din, apoteket eller sykepleieren før du bruker Xeplion. Dette legemidlet er ikke undersøkt hos eldre pasienter med demens, men eldre pasienter med demens som behandles med andre medisiner av lignende type kan ha økt risiko for hjerneslag eller død (se avsnitt 4, mulige bivirkninger).
Alle medisiner har bivirkninger, og noen av bivirkningene av dette legemidlet kan forverre symptomene på andre medisinske tilstander. Av denne grunn er det viktig at du diskuterer med legen din noen av følgende tilstander, som potensielt kan bli verre under behandling med dette legemidlet.
- Hvis du har Parkinsons sykdom.
- Hvis du noen gang har blitt diagnostisert med en sykdom hvis symptomer inkluderer høy temperatur og muskelstivhet (også kjent som Neuroleptic Malignant Syndrome).
- Hvis du noen gang har hatt unormale bevegelser i tungen eller ansiktet (Tardive Dyskinesia).
- Hvis du vet at du tidligere har hatt lave nivåer av hvite blodlegemer (som kan ha blitt forårsaket av andre medisiner).
- Hvis du er diabetiker eller disponert for diabetes.
- Hvis du har blitt diagnostisert med brystkreft eller en svulst i hypofysen i hjernen.
- Hvis du har hjertesykdom eller tar behandling for en hjertesykdom som har en tendens til å senke blodtrykket.
- Hvis du har lavt blodtrykk når du står opp eller plutselig bytter fra å ligge til å sitte.
- Hvis du lider av epilepsi.
- Hvis du har nyreproblemer.
- Hvis du har leverproblemer.
- Hvis du har en langvarig og / eller smertefull ereksjon.
- Hvis du har problemer med å kontrollere kroppstemperaturen eller overdreven varme.
- Hvis du har et unormalt høyt nivå av prolaktinhormon i blodet, eller hvis du har en mulig prolaktinavhengig svulst.
- Hvis du eller noen andre i familien din har en historie med blodpropp (trombi), ettersom antipsykotika har vært forbundet med dannelse av blodpropper.
Hvis du har noen av disse tilstandene, snakk med legen din slik at han kan vurdere om du må justere dosen din eller følge den nøye en stund.
Siden farlig lave antall av en bestemt type hvite blodlegemer som er nødvendige for å stoppe infeksjoner i blodet, har blitt observert svært sjelden hos pasienter som tar dette legemidlet, kan legen din sjekke antall hvite blodlegemer.
Selv om du tidligere har tolerert oral paliperidon eller oralt risperidon, oppstår det sjelden allergiske reaksjoner etter å ha mottatt Xeplion -injeksjoner. Se legen din umiddelbart hvis du får utslett, hevelse i halsen, kløe eller pusteproblemer, da dette kan være tegn på en alvorlig allergisk reaksjon.
Denne medisinen kan forårsake vektøkning. Betydelig vektøkning kan påvirke helsen negativt. Legen din må veie deg jevnlig.
Siden diabetes mellitus eller forverring av eksisterende diabetes mellitus har blitt observert hos pasienter som tar dette legemidlet, bør legen din sjekke om det er høyt blodsukker. Hos pasienter med eksisterende diabetes bør blodsukkernivået overvåkes regelmessig.
Siden denne medisinen kan redusere trangen til å kaste opp, er det en mulighet for at den kan maskere kroppens normale reaksjon på inntak av giftige stoffer eller andre medisinske tilstander.
Under en "øyeoperasjon" på grunn av grumling av linsen (grå stær), kan det være at pupillen (den svarte sirkelen i midten av øyet) ikke blir større etter behov. Iris (den fargede delen av øyet) kan også bli slapp under operasjonen, noe som kan forårsake skade på øyet. Hvis du planlegger å operere øyet, må du fortelle øyelegen at du bruker dette legemidlet.
Barn og ungdom
Dette legemidlet bør ikke brukes til barn og ungdom under 18 år.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Xeplion
Fortell legen din dersom du bruker, nylig har brukt eller planlegger å bruke andre legemidler.
Å ta denne medisinen med karbamazepin (antiepileptika og stemningsstabilisator) kan gjøre det nødvendig å justere dosen av dette legemidlet.
Siden denne medisinen hovedsakelig virker på hjernen, kan interferens med andre medisiner (eller alkohol) som virker på hjernen, for eksempel andre psykiatriske legemidler, opiater, antihistaminer og medisiner mot søvnforstyrrelser, forårsake en "overdrivelse av bivirkninger som søvnighet eller andre effekter. på hjernen.
Siden dette legemidlet kan senke blodtrykket, må du være forsiktig når dette legemidlet brukes sammen med andre medisiner som senker blodtrykket.
Dette legemidlet kan redusere effekten av medisiner som brukes til å behandle Parkinsons sykdom og rastløse bensyndrom (f.eks. Levodopa).
Denne medisinen kan forårsake et "elektrokardiogram (EKG) abnormitet", som er preget av en lengre periode for progresjon av en elektrisk impuls gjennom en bestemt del av hjertet (kjent som "forlengelse av" QT -intervallet "). Andre medisiner som har denne effekten inkluderer noen medisiner som brukes til å behandle hjerterytme eller for å behandle infeksjoner og andre antipsykotika. Det er viktig at du forteller legen din om medisiner du bruker for å behandle disse tilstandene.
Hvis du er disponert for å utvikle anfall, kan denne medisinen øke sjansen for å få dem. Andre medisiner som har denne effekten inkluderer noen medisiner som brukes til å behandle depresjon eller infeksjoner og andre antipsykotika. Det er viktig at du forteller legen din om medisiner du tar for å behandle disse tilstandene.
Advarsler Det er viktig å vite at:
Graviditet og amming
Rådfør deg med lege eller apotek før du bruker dette legemidlet hvis du er gravid eller ammer, tror at du kan være gravid eller planlegger å bli gravid. Du bør ikke bruke dette legemidlet under graviditet med mindre du allerede har diskutert dette med legen din. Følgende symptomer kan forekomme hos nyfødte babyer, hos mødre som har brukt paliperidon i siste trimester (siste tre måneder av svangerskapet): risting, muskelstivhet og / eller svakhet, søvnighet, uro, pusteproblemer og problemer med å mate. har noen av disse symptomene, må du kontakte legen din.
Denne medisinen kan gå fra mor til baby gjennom morsmelk og kan skade babyen. Derfor må du ikke amme hvis du bruker dette legemidlet.
Kjøring og bruk av maskiner
Svimmelhet, ekstrem tretthet og synsproblemer kan oppstå under behandling med dette legemidlet (se avsnitt 4). Dette bør tas i betraktning i tilfeller der det er nødvendig med full årvåkenhet, f.eks. Når du kjører bil eller bruker maskiner.
Viktig informasjon om noen av ingrediensene i Xeplion
Det normale doseringsområdet for dette legemidlet inneholder mindre enn 1 mmol (23 mg) natrium per dose; i praksis er det i hovedsak "natriumfritt".
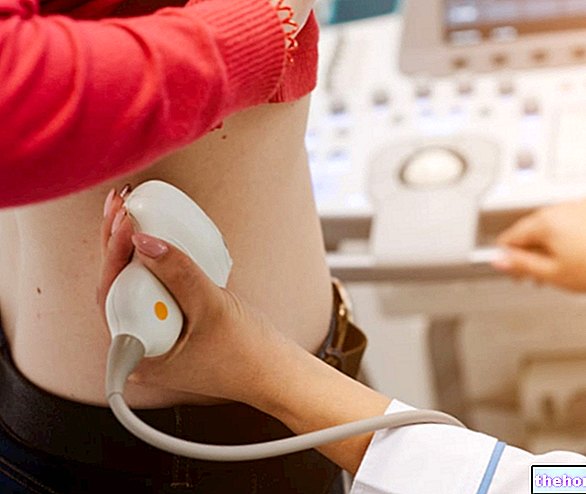
Dose, metode og administrasjonstidspunkt Hvordan bruke Xeplion: Dosering
Denne medisinen er gitt av legen din eller en annen helsepersonell på et legekontor eller en klinikk. Legen din vil bestemme når du skal gå tilbake til legekontoret eller klinikken for injeksjonen. Det er viktig å ikke hoppe over den planlagte dosen. Hvis du tror at du ikke kommer til å møte legen din, må du kontakte ham umiddelbart for å avtale en ny en. avtale så snart som mulig. Du vil bli gitt en første injeksjon (150 mg) og en annen injeksjon (100 mg) av dette legemidlet i overarmen med omtrent en ukes mellomrom. Deretter får du en injeksjon (som kan variere fra 25 mg til 150 mg) eller i overarmen eller baken en gang i måneden.
Hvis legen din bytter deg fra risperidon med forlenget frigivelse til dette legemidlet, får du din første injeksjon av dette legemidlet (som kan variere fra 25 mg til 150 mg) enten i overarmen eller baken på datoen som allerede er planlagt for din neste injeksjon . Deretter får du en injeksjon (som kan variere fra 25 mg til 150 mg) enten i overarmen eller baken en gang i måneden.
Avhengig av symptomene dine, kan legen din øke eller redusere mengden medisin du får på tidspunktet for den planlagte månedlige injeksjonen med ett dosenivå.
Pasienter med nyreproblemer
Legen din kan justere dosen av legemidlet basert på nyrefunksjonen din. Hvis du har milde nyreproblemer, kan legen forskrive en lavere dose. Hvis du har moderate til alvorlige nyreproblemer, bør denne medisinen ikke brukes.
Pensjonister
Legen din kan redusere dosen av dette legemidlet hvis nyrefunksjonen er redusert.
Overdosering Hva du skal gjøre hvis du har tatt for mye Xeplion
Hvis du har tatt for mye Xeplion
Denne medisinen vil bli gitt til deg under medisinsk tilsyn; Det er derfor lite sannsynlig at du vil bli gitt for mye.
Pasienter som har fått en overdose av paliperidon kan oppleve følgende symptomer: døsighet eller sedasjon, rask hjerterytme, lavt blodtrykk, unormalt elektrokardiogram (sporing av hjertets elektriske aktivitet) eller langsomme eller unormale bevegelser i ansikt, kropp, armer eller ben.
Hvis du slutter å bruke Xeplion
Hvis du slutter å motta injeksjoner, mister du effekten av medisinen. Du bør ikke slutte å bruke dette legemidlet med mindre legen din forteller deg det, siden symptomene dine kan komme tilbake.
Spør lege eller apotek hvis du har ytterligere spørsmål om hvordan du bruker dette legemidlet
Bivirkninger Hva er bivirkningene av Xeplion
Som alle andre legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Fortell legen din umiddelbart hvis:
- Du tror du har blodpropper i venene, spesielt i beina (symptomer inkluderer hevelse, smerter og rødhet i beina), som kan bevege seg langs blodårene til lungene og forårsake brystsmerter og pustevansker. Kontakt legen din umiddelbart hvis du merker noen av disse symptomene.
- Du har demens og merker en plutselig endring i din mentale tilstand eller en "plutselig svakhet eller nummenhet i ansikt, armer eller ben, spesielt på den ene siden, eller hvis språket ditt er uforståelig, selv om det er for kort tid. De kan." være tegn på et slag.
- Du har feber, muskelstivhet, svette eller redusert bevissthet (en lidelse som kalles "Neuroleptisk ondartet syndrom"). Umiddelbar medisinsk behandling kan være nødvendig.
- Han er mann og har langvarig eller smertefull ereksjon. Denne tilstanden kalles priapisme. Umiddelbar medisinsk behandling kan være nødvendig.
- Han har ufrivillige rytmiske bevegelser i tungen, munnen og ansiktet. Det kan være nødvendig å avbryte behandling med paliperidon.
- Du har en alvorlig allergisk reaksjon preget av feber, hevelse i munn, ansikt, lepper eller tunge, kortpustethet, kløe, utslett og noen ganger blodtrykksfall (tilsvarer en anafylaktisk reaksjon "). Tolereres oralt risperidon eller oralt paliperidon, oppstår det sjelden allergiske reaksjoner etter å ha mottatt Xeplion -injeksjoner.
Følgende bivirkninger kan oppstå:
Svært vanlige: kan ramme mer enn 1 av 10 personer
- problemer med å sovne eller å sove
- hodepine
Vanlige: kan forekomme hos opptil 1 av 10 personer
- vanlige forkjølelsessymptomer, urinveisinfeksjon, følelse av å ha influensa
- Xeplion kan øke nivåene av et hormon som kalles 'prolaktin' som finnes i en blodprøve (som kan forårsake symptomer eller ikke). Når symptomer på et høyt prolaktinnivå oppstår, kan disse inkludere (hos menn) brysthevelse, vanskeligheter med å opprettholde eller opprettholde ereksjon eller annen seksuell dysfunksjon; (hos kvinner) ubehag i brystet, tap av melk fra brystene, menstruasjonssyklus eller andre problemer med mensen
- høyt blodsukker, vektøkning, vekttap, økning i triglyserider (et fett) i blodet
- uro, depresjon, angst
- parkinsonisme: Denne tilstanden kan inkludere langsomme eller unormale bevegelser, en følelse av stivhet eller muskelspenning (gjør bevegelser rykkete), og noen ganger til og med en følelse av bevegelse som fryser og deretter starter på nytt.Andre tegn på Parkinsonisme inkluderer langsom blanding, skritt i hvile, økt spytt og / eller sikling og tap av ansiktsuttrykk.
- rastløshet, søvnighet eller tap av årvåkenhet
- dystoni: Dette er en tilstand som innebærer langsom eller langvarig ufrivillig muskelsammentrekning. Selv om det kan involvere hvilken som helst del av kroppen (noe som resulterer i unormal holdning), involverer dystoni ofte muskler i ansiktet, inkludert unormale bevegelser i øyne, munn, tunge eller kjeve
- svimmelhet
- dyskinesi: dette er en tilstand som involverer ufrivillige muskelbevegelser og kan omfatte repeterende, spastiske eller vridde bevegelser eller rykninger.
- skjelving
- lav puls, rask puls
- høyt blodtrykk
- hoste, tett nese
- magesmerter, oppkast, kvalme, forstoppelse, diaré, fordøyelsesbesvær, tannpine
- økning i levertransaminaser i blodet
- utslett
- smerter i bein eller muskler, ryggsmerter
- feber, svakhet, tretthet (tretthet)
- en reaksjon på injeksjonsstedet, inkludert kløe, smerte eller hevelse
Mindre vanlige: kan ramme opptil 1 av 100 mennesker
- lungebetennelse, brystbetennelse (bronkitt), luftveisinfeksjon, bihulebetennelse, blæreinfeksjon, ørebetennelse, øyeinfeksjon, tonsillitt, hudinfeksjon, hudbetennelse forårsaket av midd, abscess under huden
- reduksjon i antall hvite blodlegemer, anemi, reduksjon i røde blodlegemer, økning i eosinofiler i blodet (en type hvite blodlegemer)
- allergisk reaksjon
- diabetes eller forverring av diabetes, økning i blodinsulin (et hormon som kontrollerer blodsukkernivået)
- økt appetitt, tap av matlyst som resulterer i underernæring og lav kroppsvekt
- økt kolesterol i blodet
- søvnforstyrrelser, forhøyet humør (mani), forvirring, redusert seksuell trang, nervøsitet, mareritt
- tardiv dyskinesi (rykninger eller rykninger som du ikke kan kontrollere i ansiktet, tungen eller andre deler av kroppen). Kontakt legen din umiddelbart hvis du opplever ufrivillige rytmiske bevegelser i tungen, munnen og ansiktet. Det kan være nødvendig å stoppe denne medisinen
- anfall (anfall), besvimelse, et presserende behov for å bevege en del av kroppen, svimmelhet når du reiser deg, forstyrrelser i oppmerksomheten, taleproblemer, tap eller unormal smakssans, nedsatt følsomhet i huden for smerter og berøring, prikking, prikkende eller nummen følelse av huden
- tåkesyn, infeksjon i øyet eller "litt rødt", tørt øye
- spinnende følelse (svimmelhet), ringing i ørene, ørepine
- atrieflimmer (en unormal hjerterytme), en avbrudd i ledningen mellom de øvre og nedre delene av hjertet, unormal elektrisk ledning av hjertet, forlengelse av hjertets QT -intervall, rask hjerterytme når du står opp, unormal elektrisk sporing av hjertet ( elektrokardiogram eller EKG), en følelse av å løpe eller dunke i brystet (hjertebank)
- lavt blodtrykk, redusert blodtrykk når du reiser deg (som et resultat kan noen som tar dette legemidlet føle seg svake, svimmel eller besvime når de plutselig står opp eller setter seg ned)
- kortpustethet, lungestopp, tungpustethet, ondt i halsen, neseblod
- ubehag i magen, mage- eller tarminfeksjon, munntørrhet, overdreven passering av gass eller luft
- økning i GGT i blodet (et leverenzym som kalles gamma-glutamyltransferase), økning i leverenzymer i blodet
- utslett (eller elveblest), kløe, hårtap, eksem, tørr hud, rød hud, kviser
- muskelspasmer, leddstivhet, nakkesmerter, leddsmerter
- inkontinens (mangel på kontroll) av urin, hyppig vannlating, smerter ved vannlating
- erektil dysfunksjon, ejakulasjonsforstyrrelse, tap av menstruasjon, forsinket menstruasjon, fravær av menstruasjon eller andre problemer med menstruasjon (kvinner), brystutvikling hos menn, tap av morsmelk, seksuell dysfunksjon, vaginal utslipp.
- hevelse i ansikt, munn, øyne eller lepper, hevelse i kroppen, armer eller ben
- en endring i måten du går på
- brystsmerter, ubehag i brystet, kvalme
- herding av huden
- falle
Sjeldne: kan forekomme hos opptil 1 av 1000 mennesker
- soppspikerinfeksjon
- farlig lavt antall av en bestemt type hvite blodlegemer som trengs for å bekjempe infeksjoner
- reduksjon i en bestemt type hvite blodlegemer som tjener til å beskytte kroppen mot infeksjon, reduksjon i blodplater (blodceller som bidrar til å stoppe blødning)
- alvorlig allergisk reaksjon preget av feber, hevelse i munn, ansikt, lepper eller tunge, kortpustethet, kløe, utslett og noen ganger blodtrykksfall,
- upassende sekresjon av et hormon som styrer urinvolumet
- farlig overdreven vanninntak, livstruende komplikasjoner fra ukontrollert diabetes
- lavt blodsukker, overdreven vanninntak
- mangel på følelser
- manglende evne til å nå orgasme
- nevroleptisk ondartet syndrom (forvirring, redusert eller bevissthetstap, høy feber og alvorlig muskelstivhet), plutselig tap av blodtilførsel til hjernen (hjerneslag eller "mini" slag), mangel på respons på stimuli, tap av bevissthet, lavt nivå av bevissthet, forstyrrelser i balansen
- vaskulære problemer i hjernen, koma forårsaket av ukontrollert diabetes, unormal koordinasjon, skjelving i hodet
- DrDeramus (økt trykk inne i øyeeplet), problemer med øyebevegelser, øyet ruller mot baksiden av hodet, øye overfølsomhet for lys, økte tårer, røde øyne
- uregelmessig hjerteslag
- blodpropp i venene, spesielt i beina (symptomer inkluderer hevelse, smerter og rødhet i beina), som kan bevege seg langs blodårene til lungene og forårsake brystsmerter og pustevansker. Kontakt legen din umiddelbart hvis du merker noen av disse symptomene.
- redusert oksygen i deler av kroppen (fordi blodstrømmen avtar), rødme
- pusteproblemer under søvn (søvnapné), rask og grunne pust, lungebetennelse forårsaket av innånding av mat, lunger i luftveiene, stemmeforstyrrelser.
- betennelse i bukspyttkjertelen, blokkering av tarmen, hovent tunge, fekal inkontinens, veldig hard avføring, problemer med å svelge, sprukne lepper, mangel på tarmbevegelse som forårsaker blokkering
- gulfarging av hud og øyne (gulsott)
- alvorlig allergisk reaksjon med hevelse som kan påvirke halsen og forårsake pustevansker,
- legemiddelrelatert utslett, misfarging av huden, fortykning av huden, peeling og kløende hodebunn eller hud, flass
- nedbrytning av muskelfibre og muskelsmerter (rabdomyolyse), unormal holdning
- en økning i CPK (kreatinfosfokinase) i blodet, et enzym som noen ganger frigjøres når det er muskelskade, felles hevelse, muskelsvakhet
- manglende evne til å tisse
- priapisme (en langvarig ereksjon av penis som kan kreve kirurgisk behandling)
- brystsmerter, ubehag i brystet, brystforstørrelse, brystforstørrelse, brystvæske som lekker fra brystene
- veldig lav kroppstemperatur, nedgang i kroppstemperatur, frysninger, økning i kroppstemperatur, tørstfølelse, abstinenssymptomer
- akkumulering av pus forårsaket av infeksjon på injeksjonsstedet, dyp hudinfeksjon, en cyste på injeksjonsstedet, blåmerker på injeksjonsstedet
Ikke kjent: frekvensen kan ikke estimeres ut fra tilgjengelige data
- sukker i urinen Følgende bivirkninger har blitt sett ved bruk av et annet legemiddel som kalles risperidon som ligner veldig på paliperidon, så disse effektene kan også forventes med denne medisinen: andre typer hjerneblodkarproblemer, lungekrepituslyder, død hudceller på injeksjonsstedet og sår på injeksjonsstedet. Øyeproblemer kan også oppstå under grå stær kirurgi. Under kataraktkirurgi kan det oppstå en tilstand som kalles intraoperativ diskett irissyndrom (IFIS) hvis du tar eller har tatt Xeplion. Hvis du skal operere grå stær, må du fortelle legen din om du tar eller har tatt denne medisinen.
Rapportering av bivirkninger
Hvis du får bivirkninger, snakk med legen din, apoteket eller sykepleieren. Dette inkluderer mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget. Du kan også rapportere bivirkninger direkte via det nasjonale rapporteringssystemet som er oppført i vedlegg V. Bivirkninger du kan hjelpe gi mer informasjon om sikkerheten til dette legemidlet
Utløp og oppbevaring
Hold denne medisinen utilgjengelig for barn.
Bruk ikke dette legemidlet etter utløpsdatoen som er angitt på esken Utløpsdatoen refererer til den siste dagen i måneden.
Må ikke oppbevares over 30 ° C.
Ikke kast medisiner i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Sammensetning og farmasøytisk form
Hva Xeplion inneholder
Den aktive ingrediensen er paliperidon.
Hver ferdigfylte sprøyte med Xeplion 25 mg inneholder 39 mg paliperidonpalmitat.
Hver ferdigfylte sprøyte med Xeplion 50 mg inneholder 78 mg paliperidonpalmitat.
Hver ferdigfylte sprøyte med Xeplion 75 mg inneholder 117 mg paliperidonpalmitat.
Hver Xeplion 100 mg ferdigfylt sprøyte inneholder 156 mg paliperidonpalmitat.
Hver Xeplion 150 mg ferdigfylt sprøyte inneholder 234 mg paliperidonpalmitat.
Andre innholdsstoffer er: Polysorbat 20 Polyetylenglykol 4000 Sitronsyre monohydrat Di-natriumhydrogenfosfat vannfritt Natriumdihydrogenfosfatmonohydrat Natriumhydroksid (for pH-justering) Vann til injeksjonsvæsker
Hvordan Xeplion ser ut og innholdet i pakningen
Xeplion er en hvit til off-white injeksjonsvæske, suspensjon, i en ferdigfylt sprøyte.
Hver pakke inneholder 1 ferdigfylt sprøyte og 2 nåler.
Behandlingsstartpakke: Hver pakke inneholder 1 pakke Xeplion 150 mg og 1 pakke Xeplion 100 mg.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
XEPLION 100 MG FORLÆNGET RELEASE INJEKTERbar suspensjon
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hver ferdigfylte sprøyte inneholder 156 mg paliperidonpalmitat tilsvarende 100 mg paliperidon.
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Injeksjonsvæske, suspensjon, depottabletter.
Suspensjonen er hvit til off-white i fargen. Suspensjonen har en nøytral pH (ca. 7,0).
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
XEPLION er indisert for vedlikeholdsterapi av schizofreni hos voksne pasienter stabilisert på paliperidon eller risperidon.
Hos utvalgte voksne pasienter med schizofreni og som tidligere har svart på paliperidon eller oralt risperidon, kan XEPLION brukes uten forutgående oral stabilisering hvis psykotiske symptomer er milde til moderate og langtidsvirkende injiserbar behandling er nødvendig.
04.2 Dosering og administrasjonsmåte
Dosering
Det anbefales å starte XEPLION med en dose på 150 mg på dag 1 av behandlingen og en dose på 100 mg en uke senere (dag 8), i begge tilfeller administrert i deltoidmusklen for raskt å oppnå terapeutiske konsentrasjoner (se pkt.5.2 ). Den tredje dosen bør administreres en måned etter den andre dosen. Den anbefalte månedlige vedlikeholdsdosen er 75 mg; Noen pasienter kan ha fordeler av lavere eller høyere doser innenfor anbefalt område på 25-150 mg basert på subjektiv toleranse og / eller effekt. Overvektige eller overvektige pasienter kan kreve doser nær det øvre området (se pkt. 5.2). Etter den andre dosen kan månedlige vedlikeholdsdoser administreres både i deltoidmusklen og i rumpa.
"Justering av vedlikeholdsdosen kan gjøres månedlig. Når du foretar dosejusteringer, bør du vurdere de forlengede frigjøringsegenskapene til XEPLION (se pkt. 5.2), siden full effekt av vedlikeholdsdoser ikke er tydelig på flere" måneder.
Bytte fra oralt paliperidon eller oralt risperidon
I den innledende fasen av behandlingen med XEPLION kan tidligere oralt paliperidon eller oralt risperidon trekkes tilbake. XEPLION må startes som tidligere beskrevet i begynnelsen av avsnitt 4.2.
Bytte fra injiserbart risperidon til langvarig frigjøring
Når pasienter bytter fra injiserbart risperidon til forlenget frigjøring, start behandling med XEPLION i stedet for neste planlagte injeksjon. XEPLION må deretter fortsette med månedlige intervaller. Den første doseringsplanen for uke 1, som inkluderer intramuskulære injeksjoner (henholdsvis dag 1 og dag 8) som beskrevet i avsnitt 4.2 er ikke nødvendig.
Pasienter som tidligere har stabilisert seg på forskjellige doser injisert risperidon med depottabletter, kan oppnå lignende steady-state paliperidoneksponering under vedlikeholdsbehandling med månedlige doser XEPLION i henhold til følgende tidsplan:
Doser av injisert injiserbart risperidon og XEPLION kreves for å oppnå lignende steady-state paliperidoneksponering
Avbrytelse av antipsykotisk medisin bør gjøres i samsvar med passende forskrivningsinformasjon. Hvis XEPLION avbrytes, bør dets egenskaper ved langvarig frigjøring vurderes. Som også anbefalt for andre antipsykotiske medisiner, er det nødvendig å fortsette eksisterende antipsykotiske medisiner. Ekstrapyramidale symptomer (EPS , ExtraPyramidal Symptomer) bør revurderes med jevne mellomrom.
Glemt dose
Hvordan unngå å gå glipp av en dose
Det anbefales at den andre dosen av den innledende fasen av XEPLION -terapi administreres en uke etter den første dosen. For å unngå å gå glipp av en dose, kan den andre dosen gis til pasienter 4 dager før eller 4 dager etter en ukes frist (dag 8). På samme måte anbefales det etter den første fasen å gi den tredje injeksjonen og påfølgende injeksjoner en gang i måneden. For å unngå å gå glipp av en månedlig dose, kan pasienter injiseres opptil 7 dager før eller 7 dager etter den månedlige fristen.
Hvis den planlagte datoen for den andre injeksjonen av XEPLION (dag 8 ± 4 dager) har passert, avhenger den anbefalte måten å gjenoppta behandlingen av tiden som har gått siden den første injeksjonen til pasienten.
Savnet andre dose av startfasen (
Hvis det har gått mindre enn 4 uker siden den første injeksjonen, bør pasienten få den andre injeksjonen på 100 mg i deltoidmusklen så snart som mulig. En tredje 75 mg injeksjon av XEPLION i deltoid- eller setemuskelen skal gis 5 uker etter den første injeksjonen (uavhengig av når den andre injeksjonen ble gitt). Det normale månedlige injeksjonsforløpet i deltoid- eller gluteus-muskelen på 25-150 mg, basert på pasientens individuelle toleranse og / eller effekt, bør deretter følges.
Savnet andre dose av startfasen (4-7 uker etter den første injeksjonen)
Hvis det er gått 4 til 7 uker siden den første injeksjonen av XEPLION, gjenopprett doseringen med to injeksjoner på 100 mg som følger:
1. en injeksjon i deltoid så snart som mulig
2. en ny injeksjon i deltoiden en uke senere
3. gjenopptakelse av den normale månedlige injeksjonssyklusen i deltoidoid- eller gluteus-muskelen på 25-150 mg, basert på pasientens individuelle toleranse og / eller effekt.
Savnet andre dose av startfasen (> 7 uker etter første injeksjon)
Hvis det har gått mer enn 7 uker siden den første injeksjonen av XEPLION, start administrasjonen som beskrevet i anbefalingene for den innledende fasen av XEPLION angitt ovenfor.
Manglet månedlig vedlikeholdsdose (1 måned til 6 uker)
Etter den første fasen er det anbefalte injeksjonsforløpet av XEPLION månedlig. Hvis det har gått mindre enn 6 uker siden siste injeksjon, bør den tidligere angitte dosen gis så snart som mulig, etterfulgt av injeksjoner med månedlige intervaller.
Manglet månedlig vedlikeholdsdose (> 6 uker til 6 måneder)
Hvis det har gått mer enn 6 uker siden den siste injeksjonen av XEPLION, er anbefalingene som følger:
For pasienter stabilisert med doser på 25 til 100 mg:
1. en deltoidinjeksjon så snart som mulig i samme dose som pasienten tidligere ble stabilisert med
2. en ny deltoid injeksjon (samme dose) en uke senere (dag 8)
3. gjenopptakelse av den normale månedlige injeksjonssyklusen i deltoidoid- eller gluteus-muskelen på 25-150 mg, basert på pasientens individuelle toleranse og / eller effekt.
For pasienter stabilisert med 150 mg:
1. en injeksjon i deltoid så snart som mulig med en dose på 100 mg
2. nok en deltoidinjeksjon en uke senere (dag 8) i en dose på 100 mg
3. gjenopptakelse av den normale månedlige injeksjonssyklusen i deltoidoid- eller gluteus-muskelen på 25-150 mg, basert på pasientens individuelle toleranse og / eller effekt.
Manglet månedlig vedlikeholdsdose (> 6 måneder). Hvis det har gått mer enn 6 måneder siden den siste injeksjonen av XEPLION, start doseringen som beskrevet i anbefalingene for den innledende fasen av XEPLION angitt ovenfor.
Spesielle populasjoner
Eldre befolkning
Effekt og sikkerhet hos personer> 65 år er ikke fastslått.
Generelt er den anbefalte doseringen av XEPLION for eldre pasienter med normal nyrefunksjon den samme som for yngre voksne pasienter med normal nyrefunksjon. Siden eldre pasienter kan ha nedsatt nyrefunksjon, kan det imidlertid være nødvendig med dosejustering (se avsnitt Nyresvikt nedenfor for doseringsanbefalinger hos pasienter med nyreinsuffisiens).
Nyresvikt
XEPLION er ikke systematisk studert hos pasienter med nedsatt nyrefunksjon (se pkt. 5.2). For pasienter med lett nedsatt nyrefunksjon (kreatininclearance ≥ 50 til
XEPLION anbefales ikke hos pasienter med moderat eller alvorlig nedsatt nyrefunksjon (kreatininclearance
Leverinsuffisiens
Basert på erfaring med oralt paliperidon, er det ikke nødvendig med dosejustering hos pasienter med lett til moderat nedsatt leverfunksjon Siden paliperidon ikke er undersøkt hos pasienter med alvorlig nedsatt leverfunksjon, anbefales forsiktighet hos slike pasienter.
Andre spesielle populasjoner
Ingen dosejustering anbefales for XEPLION basert på kjønn, rase eller røykestatus.
Pediatrisk populasjon
Sikkerhet og effekt av XEPLION hos barn under 18 år er ikke fastslått, ingen data er tilgjengelig.
Administrasjonsmåte
XEPLION er kun til intramuskulær bruk. Det må injiseres sakte og dypt inn i muskelen. Hver injeksjon må gis av helsepersonell. Administrasjon bør skje i en enkelt injeksjon. Dosen bør ikke gis som separate injeksjoner. Dosen bør ikke administreres intravenøst eller subkutant.
Dosene på dag 1 og 8 i startfasen bør begge administreres i deltoidmusklen for raskt å oppnå terapeutiske konsentrasjoner (se pkt. 5.2). Etter den andre dosen kan månedlige vedlikeholdsdoser administreres i deltoidmusklen eller gluteus maximus. Bytte fra sete til deltoid (og omvendt) bør vurderes for smerter på injeksjonsstedet hvis slikt ubehag ikke tolereres godt (se pkt. 4.8). Det anbefales også å veksle mellom venstre og høyre side (se nedenfor).
For instruksjoner for bruk og håndtering av XEPLION, se avsnittet i pakningsvedlegget (informasjon beregnet på medisinsk eller helsepersonell).
Administrasjon i deltoidmusklen
Den anbefalte nålestørrelsen for første og vedlikeholdsadministrasjon av XEPLION i deltoidmusklen bestemmes av pasientens vekt. For en vekt ≥ 90 kg, en 1½-tommer, 22 G (38,1 mm x 0,72 mm) For en vekt på deltoidmusklene.
Administrasjon i setemuskelen
Den anbefalte nålestørrelsen for vedlikeholdsadministrasjon av XEPLION i glutealmusklen er 22 G (38,1 mm x 0,72 mm). Administrasjon bør utføres i den ytre øvre kvadranten i glutealområdet. Injeksjoner i baken må veksles mellom de to setemuskulaturen.
04.3 Kontraindikasjoner
Overfølsomhet overfor virkestoffet, overfor risperidon eller overfor noen av hjelpestoffene listet opp i pkt.6.1.
04.4 Spesielle advarsler og passende forholdsregler for bruk
Bruk hos pasienter i akutt agitasjon eller i alvorlig psykotisk tilstand
XEPLION skal ikke brukes til å håndtere akutt agitasjon eller alvorlige psykotiske tilstander når umiddelbar symptomkontroll er nødvendig.
QT -intervall
Forsiktighet bør utvises når paliperidon foreskrives hos pasienter med kjente kardiovaskulære lidelser eller med en familiehistorie med QT -forlengelse og ved samtidig bruk av andre legemidler som antas å forlenge QT -intervallet.
Neuroleptisk ondartet syndrom
Neuroleptisk ondartet syndrom (NMS), preget av hypertermi, muskelstivhet, autonom nervesystemets ustabilitet, bevissthetsendringer og forhøyet serumkreatinfosfokinase i serum, er rapportert med paliperidon. Ytterligere kliniske manifestasjoner kan omfatte myoglobinuri (rabdomyolyse) og akutt nyresvikt. Hvis en pasient viser tegn eller symptomer som tyder på NMS, bør behandling med antipsykotika, inkludert paliperidon, avbrytes.
Tardiv dyskinesi
Legemidler med antagonistisk virkning på dopaminerge reseptorer har vært assosiert med induksjon av tardiv dyskinesi preget av rytmiske og ufrivillige bevegelser, spesielt av tungen og / eller ansiktet. Avbryte antipsykotika, inkludert paliperidon.
Leukopeni, nøytropeni og agranulocytose
Hendelser av leukopeni, nøytropeni og agranulocytose har blitt rapportert ved bruk av antipsykotika, inkludert XEPLION. Agranulocytose har blitt rapportert svært sjelden (hvite blodlegemer (WBC) eller legemiddelindusert leukopeni / nøytropeni bør overvåkes under overvåking etter markedsføring). de første månedene av behandlingen og seponering av XEPLION bør vurderes ved første tegn på klinisk signifikant nedgang i WBC i fravær av andre årsaksfaktorer Pasienter med klinisk signifikant nøytropeni bør overvåkes nøye for feber eller andre symptomer eller tegn på infeksjon og behandles umiddelbart hvis slike symptomer eller tegn oppstår Pasienter med alvorlig nøytropeni (absolutt nøytrofiltall
Hyperglykemi og diabetes mellitus
Hyperglykemi, diabetes mellitus og forverring av eksisterende diabetes er rapportert under behandling med paliperidon. I noen tilfeller har tidligere vektøkning blitt rapportert som kan være en predisponerende faktor. Forbindelsen med ketoacidose er rapportert svært sjelden og sjelden med diabetisk koma. Passende klinisk overvåking anbefales i samsvar med retningslinjene som brukes for antipsykotika. Pasienter behandlet med atypiske antipsykotika, inkludert XEPLION, bør overvåkes for symptomer på hyperglykemi. (Som f.eks. polydipsi, polyuri, polyfagi og svakhet) og pasienter med diabetes mellitus bør overvåkes regelmessig for forverret glykemisk kontroll.
Vektøkning
Det er rapportert om betydelig vektøkning under bruk av XEPLION. Vekt bør evalueres regelmessig.
Hyperprolaktinemi
Cellekulturstudier antyder at cellevekst i brystkreft hos mennesker kan stimuleres av prolaktin. Selv om det ikke er påvist noen klar sammenheng med administrering av antipsykotika i kliniske og epidemiologiske studier, anbefales forsiktighet hos pasienter med relevant medisinsk historie. Paliperidon bør brukes med forsiktighet hos pasienter med mulige prolaktinavhengige svulster.
Ortostatisk hypotensjon
Paliperidon kan forårsake ortostatisk hypotensjon hos noen pasienter på grunn av dets alfablokkerende virkning.
Basert på sammenslåtte data fra tre placebokontrollerte, 6 ukers, faste doser med orale paliperidontabletter (3, 6, 9 og 12 mg), ble ortostatisk hypotensjon rapportert av 2,5% av pasientene som ble behandlet med oralt paliperidon mot 0,8% av pasientene som ble behandlet med placebo. XEPLION bør brukes med forsiktighet hos pasienter med kjent kardiovaskulær sykdom (f.eks. hjertesvikt, hjerteinfarkt eller iskemi, ledningsdefekter), cerebrovaskulær sykdom eller tilstander som disponerer pasienten for hypotensjon (f.eks. dehydrering og hypovolemi).
Kramper
XEPLION bør brukes med forsiktighet hos pasienter som tidligere har hatt anfall eller andre tilstander som kan senke anfallsterskelen.
Nyresvikt
Plasmakonsentrasjonen av Paliperidon øker hos pasienter med nedsatt nyrefunksjon, og derfor anbefales dosejustering hos pasienter med mild nyreinsuffisiens. XEPLION anbefales ikke hos pasienter med moderat eller alvorlig nedsatt nyrefunksjon (kreatininclearance
Leverinsuffisiens
Det er ingen tilgjengelige data om pasienter med alvorlig nedsatt leverfunksjon (Child-Pugh klasse C). Forsiktighet utvises ved bruk av paliperidon hos slike pasienter.
Eldre pasienter med demens
Det er ikke utført studier med XEPLION hos eldre pasienter med demens. XEPLION bør brukes med forsiktighet hos eldre pasienter med demens med risikofaktorer for slag. Erfaringen med risperidon nevnt nedenfor anses også som gyldig for paliperidon.
Global dødelighet
I en metaanalyse av 17 kontrollerte kliniske studier hadde eldre demenspasienter behandlet med andre atypiske antipsykotika, inkludert risperidon, aripiprazol, olanzapin og quetiapin, en høyere risiko for dødelighet enn placebo. Blant de som ble behandlet med risperidon, var dødeligheten 4% sammenlignet med 3,1% for placebo.
Cerebrovaskulære bivirkninger
En omtrent tre ganger økt risiko for cerebrovaskulære bivirkninger ble observert i randomiserte placebokontrollerte kliniske studier hos demenspasienter behandlet med noen atypiske antipsykotika, inkludert risperidon, aripiprazol og olanzapin. Mekanismen bak den økte risikoen er ukjent.
Parkinsons sykdom og demens med Lewy -kropper
Leger bør veie risikoen og fordelene ved å forskrive XEPLION til pasienter med Parkinsons sykdom eller demens med Lewy -legemer (DLB) ettersom begge pasientgruppene kan ha større risiko for å utvikle nevroleptisk ondartet syndrom, samt vise økt følsomhet overfor antipsykotika. Manifestasjoner av denne økte følsomheten kan omfatte forvirring, sløvhet, postural ustabilitet med hyppige fall, samt ekstrapyramidale symptomer.
Priapisme
Antipsykotiske legemidler (inkludert risperidon) med alfa-adrenerge blokkerende effekter har blitt rapportert å forårsake priapisme. Under overvåking etter markedsføring er det også rapportert priapisme med oral paliperidon, som er den aktive metabolitten av risperidon. Pasienter bør informeres om at hvis priapisme ikke forsvinner innen 3-4 timer, bør de søke øyeblikkelig medisinsk hjelp.
Kroppstemperaturregulering
Svekket kroppens evne til å senke kroppstemperaturen har blitt tilskrevet antipsykotiske legemidler. Spesiell forsiktighet anbefales ved forskrivning av XEPLION til pasienter som kan bli utsatt for forhold som kan bidra til en økning i kroppstemperaturen, for eksempel hard trening, eksponering for ekstrem varme, samtidig behandling av antikolinerge legemidler eller utsatt for dehydrering.
Venøs tromboembolisme
Tilfeller av venøs tromboembolisme (VTE) er rapportert med antipsykotiske legemidler.
Pasienter behandlet med antipsykotika har ofte ervervet risikofaktorer for VTE, derfor må alle mulige risikofaktorer for VTE identifiseres før og under behandling med XEPLION og forebyggende tiltak iverksettes.
Antiemetisk effekt
En antiemetisk effekt ble observert i prekliniske studier med paliperidon. Denne effekten, hvis den forekommer hos mennesker, kan maskere tegn og symptomer på overdosering av visse medisiner eller tilstander som tarmobstruksjon, Reye syndrom og hjernesvulst.
Administrasjon
Det må utvises forsiktighet for å unngå utilsiktet injeksjon av XEPLION i et blodkar.
Intraoperativt Floppy Iris syndrom
Intraoperativt Floppy Iris syndrom (IFIS) har blitt observert under kataraktkirurgi hos pasienter behandlet med legemidler med alfa1a-adrenerg antagonisteffekt, for eksempel XEPLION (se pkt. 4.8).
IFIS kan øke risikoen for okulære komplikasjoner under og etter operasjonen. Nåværende eller tidligere bruk av legemidler med alfa1a-adrenerge antagonistvirkning bør gjøres kjent for øyekirurgen før operasjonen. Den potensielle fordelen med å avbryte behandling med alfa1 -blokkering før kataraktkirurgi er ikke fastslått og må avveies mot risikoen for å avbryte antipsykotisk behandling.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Forsiktighet utvises ved forskrivning av XEPLION i kombinasjon med legemidler som er kjent for å forlenge QT -intervallet, for eksempel klasse IA antiarytmika (f.eks. Kinidin, disopyramid) og klasse III antiarytmika (f.eks. Amiodaron, sotalol), noen antihistaminer, noen andre antipsykotika og noen malariaer (f.eks. mefloquine). Listen er veiledende og ikke uttømmende.
Potensial for XEPLION å påvirke andre medisiner
Paliperidon forventes ikke å forårsake klinisk signifikante farmakokinetiske interaksjoner med legemidler som metaboliseres av cytokrom P-450 isoenzymer.
Gitt effektene av paliperidon på primær sentralnervesystem (CNS) (se pkt. 4.8), bør XEPLION brukes med forsiktighet i kombinasjon med andre sentralvirkende legemidler, f.eks. angstdempende, de fleste antipsykotika, hypnotika, opiater, etc. eller med alkohol.
Paliperidon kan motvirke effekten av levodopa og andre dopaminagonister.Hvis denne kombinasjonen anses nødvendig, spesielt i den avsluttende fasen av Parkinsons sykdom, bør den laveste effektive dosen av hver behandling foreskrives.
På grunn av dets potensial til å indusere ortostatisk hypotensjon (se pkt. 4.4), kan en additiv effekt observeres når XEPLION administreres med andre terapeutiske midler som har dette potensialet, f.eks. Andre antipsykotika eller trisykliske midler.
Forsiktighet tilrådes hvis paliperidon administreres i kombinasjon med andre legemidler som antas å senke anfallsterskelen (f.eks. Fenotiaziner eller butyrofenoner, tricykliske eller SSRI -er, tramadol, mefloquin, etc.).
Samtidig administrering av paliperidon depottabletter ved steady state (12 mg én gang daglig) med depottabletter av valproinsyre + valproatnatrium (500 til 2000 mg én gang daglig) påvirket ikke farmakokinetikken til valproat i steady state.
Det er ikke utført interaksjonsstudier mellom XEPLION og litium, men en farmakokinetisk interaksjon er usannsynlig.
Potensial for andre medisiner for å påvirke XEPLION
utdanning in vitro indikerer at CYP2D6 og CYP3A4 kan være minimalt involvert i metabolismen av paliperidon, men det er ingen indikasjoner eller in vitro ingen in vivo at disse isoenzymer spiller en betydelig rolle i metabolismen av paliperidon. Samtidig administrering av oralt paliperidon og paroksetin, en kraftig hemmer av CYP2D6, viste ikke klinisk signifikante effekter på paliperidons farmakokinetikk.
Samtidig administrering av paliperidon med forlenget frigjøring en gang daglig med karbamazepin 200 mg to ganger daglig forårsaket en ca 37% reduksjon i gjennomsnittlig Cmax og AUC ved stabil av paliperidon. Denne nedgangen er vesentlig forårsaket av en 35% økning i nyreclearance av paliperidon sannsynligvis som følge av karbamazepininduksjon av renal P-gp. En mindre reduksjon i mengden av virkestoffet som utskilles uendret i urinen antyder en minimal effekt på CYP-metabolismen eller biotilgjengeligheten av paliperidon under samtidig administrering med karbamazepin Med høyere doser karbamazepin kan det oppstå større reduksjoner i plasmakonsentrasjoner av paliperidon Ved initiering av karbamazepinbehandling bør dosen av XEPLION revurderes og økes om nødvendig. Omvendt, ved seponering av karbamazepinbehandling, bør dosen av XEPLION revurderes og reduseres om nødvendig.
Samtidig administrering av en enkelt dose på en 12 mg oral forlenget paliperidontablett med valproinsyre + natriumvalproat depottabletter (to 500 mg tabletter en gang daglig) resulterte i en økning på omtrent 50% paliperidon Cmax og AUC, muligens som et resultat av økt oral absorpsjon. Siden det ikke ble observert noen effekt på systemisk clearance, ville det ikke forventes en klinisk signifikant interaksjon mellom valproinsyre depottabletter + natriumvalproat og XEPLION intramuskulær injeksjon Denne interaksjonen er ikke undersøkt med XEPLION.
Samtidig bruk av XEPLION og risperidon
Risperidon administrert oralt eller intramuskulært vil bli metabolisert til paliperidon i ulik grad. Vær forsiktig hvis oral risperidon eller paliperidon administreres samtidig med XEPLION.
04.6 Graviditet og amming
Svangerskap
Det er ingen tilstrekkelige data om bruk av paliperidon under graviditet Paliperidonpalmitat injisert intramuskulært og paliperidon administrert oralt har ikke vist seg å være teratogent i dyreforsøk, men andre typer reproduksjonstoksisitet er observert (se pkt. 5.3). Nyfødte utsatt for antipsykotika (inkludert paliperidon) i tredje trimester av svangerskapet har risiko for bivirkninger, inkludert ekstrapyramidale og / eller abstinenssymptomer som kan variere i alvorlighetsgrad og varighet etter fødselen. rastløshet, hypertoni, hypotoni, tremor, søvnighet, pustevansker eller spiseforstyrrelser . Følgelig må spedbarn overvåkes nøye. XEPLION skal ikke tas under graviditet med mindre det er absolutt nødvendig.
Foringstid
Paliperidon skilles ut i morsmelk i en slik grad at effekter på det ammede barnet er sannsynlig når terapeutiske doser gis til ammende kvinner. XEPLION skal ikke brukes i ammeperioden.
Fruktbarhet
Ingen relevante effekter ble observert i ikke-kliniske studier.
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Paliperidon kan påvirke evnen til å kjøre bil eller bruke maskiner lett eller moderat på grunn av potensielle nervesystem og visuelle effekter som sedasjon, søvnighet, synkope og tåkesyn (se pkt. 4.8). Derfor bør pasienter rådes til ikke å kjøre bil eller bruke maskiner før individuell følsomhet for XEPLION er kjent.
04.8 Bivirkninger
Oppsummering av sikkerhetsprofilen
De hyppigst rapporterte bivirkningene i kliniske studier var søvnløshet, hodepine, angst, øvre luftveisinfeksjon, reaksjon på injeksjonsstedet, parkinsonisme, vektøkning, akatisi, uro, sedasjon / søvnighet., Kvalme, forstoppelse, svimmelhet, muskel -skjelett smerter, takykardi, tremor, magesmerter, oppkast, diaré, tretthet og dystoni. Av disse synes akatisi og sedasjon / søvnighet å være doserelatert.
Tabell over bivirkninger
Følgende bivirkninger er alle rapportert med paliperidon etter frekvenskategori estimert fra kliniske studier av XEPLION. Følgende vilkår og frekvenser gjelder: veldig vanlig (≥ 1/10), felles (≥ 1/100 til uvanlig (≥ 1/1000 til sjeldne (≥ 1/10 000 til svært sjeldne (ikke kjent (kan ikke estimeres ut fra tilgjengelige data fra kliniske studier)).
a Se "hyperprolaktinemi" nedenfor.
b Se "ekstrapyramidale symptomer" nedenfor.
c I placebokontrollerte kliniske studier ble diabetes mellitus rapportert hos 0,32% av pasientene behandlet med XEPLION sammenlignet med 0,39% i placebogruppen. Den totale forekomsten av alle kliniske studier var 0,47% hos alle pasienter behandlet med XEPLION.
d Søvnløshet inkluderer: første søvnløshet, sentral søvnløshet; anfall inkluderer: grand mal -anfall; ødem inkluderer: generalisert ødem, perifert ødem, plastisk ødem; menstruasjonsforstyrrelse inkluderer: uregelmessig menstruasjon, oligomenoré
e Ikke observert i kliniske studier av XEPLION, men observert etter markedsføring med paliperidon.
Bivirkninger rapportert med risperidonformuleringer
Paliperidon er den aktive metabolitten av risperidon, derfor er bivirkningsprofilene til disse forbindelsene (inkludert både orale og injiserbare formuleringer) relevante for hverandre. I tillegg til bivirkningene nevnt ovenfor, har følgende bivirkninger blitt rapportert ved bruk av risperidonprodukter og kan forventes med XEPLION.
Nevrologiske sykdommer: cerebrovaskulære lidelser
Øyesykdommer: sflag iris syndrom (intraoperativt)
Åndedrettsorganer, thorax og mediastinum: rales
Generelle lidelser og tilstander på administrasjonsstedet (observert med injiserbar formulering av risperidon): nekrose på injeksjonsstedet, sår på injeksjonsstedet.
Beskrivelse av utvalgte bivirkninger
Anafylaktisk reaksjon
Tilfeller av anafylaktisk reaksjon etter injeksjon med XEPLION er sjelden rapportert etter markedsføring hos pasienter som tidligere har tolerert oral risperidon eller oralt paliperidon.
Reaksjoner på injeksjonsstedet
Den vanligste rapporterte bivirkningen på injeksjonsstedet var smerter. Flertallet av disse rapporterte reaksjonene var milde til moderate. Forsøkspersoners rangering av smerter på injeksjonsstedet basert på en visuell analog skala hadde en tendens til å minke over tid i frekvens og intensitet i alle fase 2 og fase 3. Studier av Deltoid -injeksjoner ble oppfattet som mildt smertefulle. Større enn de tilsvarende injeksjonene i baken. Andre reaksjoner på injeksjonsstedet var stort sett milde i intensitet og inkluderte indurasjon (vanlig), kløe (uvanlig) og knuter (sjelden).
Ekstrapyramidale symptomer (EPS)
EPS inkluderte en samlet analyse av følgende begreper: parkinsonisme (inkluderer spyttoverskytning, stivhet i muskuloskeletalen, parkinsonisme, tap av spytt, tannhjulstivhet, bradykinesi, hypokinesi, maskefasader, muskelspenninger, akinesi, nukal stivhet, muskelstivhet, parkinsonistisk gang og unormal glabellar refleks, Parkinsons tremor i hvile), akatisi (inkluderer akatisi, rastløshet, hyperkinesi, rastløse bensyndrom), dyskinesi (inkluderer dyskinesi, muskeltrekk, koreoatetose, athetose og myokloni), dystoni (inkluderer dystoni, hypertoni, torticollis, ufrivillige muskelsammentrekninger, muskelkontraktur, blefarospasme, okulogyrasjon, lingual lammelse, ansiktspasmer, laryngospasme, myotoni, opisthotonus, orofaryngeal spasme, pleurototonus, lingual spasme og trismus) og tremor. Det skal bemerkes at et bredere spekter av symptomer er inkludert som ikke nødvendigvis har ekstrapyramidal opprinnelse
Vektøkning
I 13-ukers studien som involverte innledende administrering av 150 mg, viste andelen personer med unormal vektøkning ≥ 7% en doserelatert trend, med en forekomst på 5% i placebogruppen sammenlignet med prosentene på 6%, 8% og 13% i henholdsvis XEPLION 25 mg, 100 mg og 150 mg grupper.
I løpet av den 33 ukers åpne overgangs- / vedlikeholdsperioden i den langsiktige tilbakefallsforebyggende studien, opplevde 12% av pasientene som ble behandlet med XEPLION denne effekten (≥ 7% vektøkning fra dobbeltblind fase til endepunkt); gjennomsnitt (SD) vektendringen fra baseline i den åpne merkefasen var + 0,7 kg.
Hyperprolaktinemi
I kliniske studier ble medianøkninger av serumprolaktin observert hos begge kjønn som fikk XEPLION. Bivirkninger som kan tyde på en økning i prolaktinnivåer (f.eks. Amenoré, galaktoré, menstruasjonsforstyrrelser, gynekomasti) er generelt rapportert i
Kategori effekter
QT -intervallforlengelse, ventrikulære arytmier (ventrikelflimmer, ventrikulær takykardi), plutselig uforklarlig død, hjertestans og torsades de pointes kan forekomme ved administrering av antipsykotika. Tilfeller av venøs tromboembolisme, inkludert tilfeller av lungeemboli og tilfeller av dyp venetrombose (frekvens ikke kjent).
Rapportering av mistenkte bivirkninger
Rapportering av mistenkte bivirkninger som oppstår etter godkjenning av legemidlet er viktig, da det muliggjør kontinuerlig overvåking av nytte / risiko -balansen for legemidlet Helsepersonell bes rapportere alle mistenkte bivirkninger via det nasjonale rapporteringssystemet. I "Vedlegg V .
04.9 Overdosering
Generelt er de forventede tegnene og symptomene på grunn av en forbedring av de kjente farmakologiske effektene av paliperidon, f.eks. Søvnighet og sedasjon, takykardi og hypotensjon, forlengelse av QT og ekstrapyramidale symptomer. Torsade de pointes og ventrikkelflimmer er rapportert hos en pasient i overdose med oralt paliperidon. Ved akutt overdose bør det tas hensyn til muligheten for flere legemidler.
Legemidlets langvarige frigivelse og den lange eliminasjonshalveringstiden for paliperidon bør vurderes ved vurdering av behandlingsbehov og restitusjon. Det er ingen spesifikk motgift mot paliperidon. Egnede generelle støttetiltak bør iverksettes. Etablere og opprettholde en fri luftvei og sikre tilstrekkelig oksygenering og ventilasjon.
Kardiovaskulær overvåking bør startes umiddelbart og bør omfatte kontinuerlig elektrokardiografisk overvåking for mulige arytmier. Hypotensjon og sirkulasjonskollaps bør behandles med passende tiltak som intravenøs væske og / eller sympatomimetiske midler. Ved alvorlige ekstrapyramidale symptomer bør antikolinerge midler administreres. Fortsett nøye overvåking og medisinsk tilsyn til pasienten er frisk.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: psykoleptika, andre antipsykotika.
ATC -kode: N05AX13.
XEPLION inneholder en racemisk blanding av (+) - og ( -) - paliperidon.
Virkningsmekanismen
Paliperidon er et selektivt blokkeringsmiddel for monoamineffekter, hvis farmakologiske egenskaper er forskjellige fra tradisjonelle nevroleptika. Paliperidon binder seg sterkt til de serotonergiske og dopaminerge D2 5-HT2 reseptorene. Paliperidon blokkerer også alfa 1-adrenerge reseptorer og i mindre grad H1-histaminergiske og alfa 2-adrenerge reseptorer. Den farmakologiske aktiviteten til (+) og (-) enantiomerene til paliperidon er kvalitativt og kvantitativt lik.
Paliperidon binder seg ikke til kolinerge reseptorer. Selv om paliperidon er en sterk D2 -antagonist, som antas å lindre de positive symptomene på schizofreni, forårsaker det mindre katalepsi og reduserer motorisk kapasitet i mindre grad enn tradisjonelle nevroleptika. Sentral dominerende serotoninantagonisme kan redusere paliperidons tendens til å forårsake ekstrapyramidale bivirkninger.
Klinisk effekt
Akutt behandling av schizofreni
Effekten av XEPLION ved akutt behandling av schizofreni ble fastslått i fire kortvarige (en 9-ukers og tre 13-ukers) dobbeltblindede, randomiserte, placebokontrollerte, faste dosestudier hos sykehusinnlagte forverrede voksne pasienter som møtte DSM -IV kriterier for schizofreni. Faste doser av XEPLION i disse studiene ble administrert på dag 1, 8 og 36 i 9-ukers studien og også på dag 64 i 13-ukers studier. Ingen ytterligere tilskudd var nødvendig. Av orale antipsykotika under akutt behandling av schizofreni med XEPLION. Det primære effektpunktet ble definert som en reduksjon i den totale poengsummen for positivt og negativt syndrom (PANSS) som vist i tabellen nedenfor. PANSS-skalaen er et multi-element validert verktøy som består av fem dimensjoner å vurdere positive symptomer, negative symptomer, konseptuell uorganisering, fiendtlighet / uro n på kontrollert og angst / depresjon. Funksjonen ble vurdert ved hjelp av skalaen Personal and Social Performance (PSP). PSP er en klinisk validert skala som måler personlig og sosial funksjon i fire domener: sosialt nyttige aktiviteter (arbeid og studier), personlige og sosiale relasjoner, egenomsorg og forstyrrende og aggressiv atferd.
I en 13-ukers studie (n = 636) som sammenlignet tre faste doser XEPLION (første deltoidinjeksjon på 150 mg etterfulgt av 3 rumpe- eller deltoiddoser på 25 mg / 4 uker, 100 mg / 4 uker eller 150 mg / 4 uker) med placebo var alle tre dosene XEPLION bedre enn placebo for å forbedre PANSS total score. I denne studien viste både behandlingsgruppene på 100 mg / 4 uker og 150 mg / 4 uker, men ikke 25 mg / 4 uker, statistisk overlegenhet i forhold til placebo for PSP -poengsummen. Disse resultatene støtter effekt og forbedring av PANSS i full varighet og ble sett tidlig på dag 4 med betydelig separasjon fra placebo i XEPLION 25 mg og 150 mg gruppene fra dag 8.
Resultatene fra de andre studiene ga statistisk signifikante resultater til fordel for XEPLION, med unntak av dosen på 50 mg i en enkelt studie (se tabellen nedenfor).
* For studie R092670-PSY-3007 ble en startdose på 150 mg administrert på dag 1 til alle pasienter i XEPLION-behandlingsgruppene etterfulgt av den tildelte dosen deretter.
Merk: Negativ endring i poengsummen indikerer forbedring.
Opprettholdelse av symptomkontroll og forsinkelse i tilbakefall av schizofreni
Effekten av XEPLION for å opprettholde symptomkontroll og forsinke tilbakefall av schizofreni ble fastslått i en lengre, dobbeltblind, placebokontrollert, fleksibel dose-studie med 849 ikke-eldre voksne personer som oppfylte DSM-IV-kriteriene for schizofreni.Denne studien inkluderte en åpen akutt behandlings- og stabiliseringsfase på 33 uker, en placebokontrollert dobbeltblind randomiseringsfase for å observere eventuelt tilbakefall og en åpen forlengelsesperiode på 52 uker. I denne studien inkluderte doser XEPLION 25 , 50, 75 og 100 mg administrert månedlig; dosen på 75 mg var bare tillatt i den 52 ukers lange forlengelsesperioden. Emner fikk i utgangspunktet fleksible doser (25-100 mg) XEPLION i en overgangsperiode. På 9 uker, etterfulgt av en vedlikeholdsperiode på 24 uker, hvor pasientene måtte ha en PANSS -score ≤ 75. Dosejusteringer var bare tillatt i de første 12 ukene av vedlikeholdsperioden. Totalt 410 stabiliserte pasienter ble randomisert til XEPLION (median varighet 171 dager [område 1 dag til 407 dager]) eller placebo (median varighet 105 dager [intervall 8 dager til 441 dager]) inntil de hadde en gjentakelse av schizofreni-symptomer i den dobbeltblindede fasen av variabel varighet. Forsøket ble stoppet tidlig av effektivitetshensyn ettersom det ble observert en signifikant lengre tid til tilbakefall (s
Pediatrisk populasjon
Det europeiske legemiddelkontoret (European Medicines Agency) har frafalt forpliktelsen til å levere resultatene av studier med XEPLION i alle undergrupper av den pediatriske populasjonen ved schizofreni. Se avsnitt 4.2 for informasjon om pediatrisk bruk.
05.2 "Farmakokinetiske egenskaper
Absorpsjon og distribusjon
Paliperidonpalmitat er palmitatesterprodusenten til paliperidon. På grunn av sin ekstremt lave vannløselighet, oppløses paliperidonpalmitat sakte etter intramuskulær injeksjon før det hydrolyseres til paliperidon og absorberes i systemisk sirkulasjon. Etter en enkelt intramuskulær dose, øker plasmakonsentrasjonen av paliperidon gradvis for å nå maksimal plasmakonsentrasjon ved en median T på 13 dager. Frigivelsen av det aktive stoffet begynner allerede på dag 1 og varer i minst 4 måneder.
Etter intramuskulær injeksjon av enkeltdoser (25-150 mg) i deltoidmusklen, ble det i gjennomsnitt observert en 28% høyere Cmax sammenlignet med injeksjon i baken. De to første intramuskulære deltoidinjeksjonene på 150 mg på dag 1 og 100 mg på dag 8 bidrar til å oppnå terapeutiske konsentrasjoner raskt. Frigjøringsprofilen og doseringsregimet for XEPLION fører til vedvarende terapeutiske konsentrasjoner. Den totale eksponeringen av paliperidon etter administrering av XEPLION var dose proporsjonal over et doseområde på 25-150 mg, og mindre enn proporsjonalt for C for doser som overstiger 50 mg. mg var 1,8 etter administrering i baken og 2,2 etter administrering i deltoid. 25-150 mg doseområde varierte fra 25 til 49 dager.
Den absolutte biotilgjengeligheten av paliperidonpalmitat etter administrering av XEPLION er 100%.
Etter administrering av paliperidonpalmitat, interkonverterer (+) og (-) enantiomerene av paliperidon, og oppnådde et AUC (+) / (-) forhold på omtrent 1,6-1,8.
Plasmaproteinbindingen av racemisk paliperidon er 74%.
Biotransformasjon og eliminering
Etter en uke etter administrering av en oral oral 1 mg dose med 14C-paliperidon med umiddelbar frigjøring, ble 59% av dosen utskilt uendret i urinen, noe som viser at paliperidon ikke metaboliseres i stor utstrekning av leveren. Omtrent 80% av administrert radioaktivitet ble gjenopprettet i urinen og 11% i avføringen. In vivo Fire metabolske veier ble identifisert, hvorav ingen utgjorde mer enn 6,5% av dosen: dealkylering, hydroksylering, dehydrogenering og benzisoksazol -spaltning. Selv om studiene in vitro har foreslått en rolle for CYP2D6 og CYP3A4 i metabolismen av paliperidon, er det ingen bevis in vivo at disse isoenzymer spiller en betydelig rolle i metabolismen av paliperidon. Befolkningsfarmakokinetiske analyser indikerer at det ikke er noen merkbar forskjell i den tilsynelatende clearance av paliperidon etter administrering av oralt paliperidon mellom omfattende metaboliserere og dårlige metaboliserere av CYP2D6 -substrater. Studier in vitro på menneskelige levermikrosomer viste at paliperidon ikke vesentlig hemmer metabolismen av legemidler som metaboliseres av cytokrom P450 isoenzymer, inkludert CYP1A2, CYP2A6, CYP2C8 / 9/10, CYP2D6, CYP2E1, CYP3A4 og CYP3A5.
Studier in vitro vist at paliperidon er et P-gp-substrat og en svak hemmer av P-gp ved høye konsentrasjoner. Ingen data er tilgjengelige in vivo og den kliniske relevansen er ukjent.
Paliperidonpalmitatinjeksjon med forlenget frigjøring versus paliperidon med oral frigjøring forlenget
XEPLION ble utviklet for å frigjøre paliperidon over en periode på en måned, mens oral paliperidon med oral forlengelse administreres daglig. Startfasebehandlingen for XEPLION (150 mg / 100 mg i deltoidmusklen på dag 1 / dag 8) ble utviklet for raskt å oppnå paliperidonkonsentrasjoner ved stabil i begynnelsen av behandlingen uten bruk av oralt tilskudd.
Generelt var de totale plasmanivåene i den innledende fasen med XEPLION innenfor eksponeringsområdet observert med 6-12 mg oral paliperidon med depottabletter. Bruk av XEPLION innledende fase-regime tillot pasienter å forbli innenfor dette 6-12 mg orale paliperidon-eksponeringsvinduet peroralt, selv i dagene med lav konsentrasjon før dosering (dag 8 og dag 36). På grunn av forskjellen i median farmakokinetiske profiler mellom de to legemidlene, bør det utvises forsiktighet når en direkte sammenligning av deres farmakokinetiske egenskaper gjøres.
Leverinsuffisiens
Paliperidon metaboliseres ikke i stor grad i leveren. Selv om XEPLION ikke er undersøkt hos pasienter med nedsatt leverfunksjon, er det ikke nødvendig med dosejustering hos pasienter med lett til moderat nedsatt leverfunksjon. I en studie med oralt paliperidon hos personer med moderat nedsatt leverfunksjon (Child-Plugh klasse B) var plasmakonsentrasjonene av fritt paliperidon lik de hos friske personer. Det er ikke utført studier med paliperidon hos pasienter med alvorlig nedsatt leverfunksjon.
Nyresvikt
Disposisjonen av en enkelt oral dose av paliperidon 3 mg depottabletter har blitt studert hos personer med varierende grad av nyrefunksjon. Eliminasjonen av paliperidon ble redusert etter hvert som den estimerte kreatininclearance minket.Den totale clearance av paliperidon ble redusert med gjennomsnittlig 32% hos personer med lett nedsatt nyrefunksjon (CrCl = 50 til
Pensjonister
Ingen dosejustering anbefales kun basert på alder. Dosejustering kan imidlertid være nødvendig på grunn av aldersrelaterte reduksjoner i kreatininclearance (se Nedsatt nyrefunksjon ovenfor og pkt.4.2).
Vekt
Farmakokinetiske studier med paliperidonpalmitat har noen ganger vist lavere (10-20%) plasmakonsentrasjoner av paliperidon hos overvektige eller overvektige pasienter enn hos pasienter med normal vekt (se pkt. 4.2).
Løp
Befolkningsfarmakokinetiske analyser av data fra studier med oralt paliperidon avslørte ingen raselaterte forskjeller i farmakokinetikken til paliperidon etter administrering av XEPLION.
Kjønn
Det ble ikke observert noen klinisk signifikante forskjeller mellom mannlige og kvinnelige pasienter.
Røyk
Basert på studier in vitro utført ved bruk av humane leverenzymer, er paliperidon ikke et substrat for CYP1A2; røyking forventes derfor ikke å ha noen effekt på paliperidons farmakokinetikk. En populasjonsfarmakokinetisk analyse av data med paliperidon depottabletter viste noe lavere paliperidoneksponering hos røykere enn hos ikke-røykere. Imidlertid er det lite sannsynlig at forskjellen er klinisk relevant. Røyking er ikke evaluert for XEPLION.
05.3 Prekliniske sikkerhetsdata
Toksisitetsstudier ved gjentatt dosering av intramuskulært injisert paliperidonpalmitat og oralt administrert paliperidon hos rotter og hunder har hovedsakelig vist farmakologiske effekter, slik som sedasjon og prolaktinmedierte effekter på bryst og kjønns kjertler. En inflammatorisk reaksjon på det intramuskulære injeksjonsstedet ble observert hos dyr behandlet med paliperidonpalmitat. Av og til har det dannet seg en abscess.
I rottereproduksjonsstudier med oralt risperidon, som i stor grad omdannes til paliperidon hos rotter og mennesker, ble det observert negative effekter på fødselsvekt og avkoms overlevelse. Ingen embryotoksisitet eller misdannelser ble observert etter intramuskulær administrering av paliperidonpalmitat til gravide rotter opp til den høyeste dosen (160 mg / kg / dag) tilsvarende 4,1 ganger eksponeringsnivået for mennesker ved maksimal anbefalt dose på 150 mg. Andre dopaminantagonister, når administrert til drektige dyr, forårsaket negative effekter på læring og motorisk utvikling hos avkom.
Paliperidonpalmitat og paliperidon var ikke gentoksiske. I orale kreftfremkallende studier av risperidon hos rotter og mus ble det funnet økninger i hypofyseadenomer (hos mus), endokrine bukspyttkjertelenadenomer (hos rotter) og brystkjertelenadenomer (hos begge artene). Det kreftfremkallende potensialet for intramuskulært injisert paliperidonpalmitat ble evaluert hos rotter. Det var en statistisk signifikant økning i brystkjerteladenokarsinomer hos hunnrotter på 10, 30 og 60 mg / kg / måned. En statistisk signifikant økning i brystkjertelen adenomer og karsinomer har blitt påvist hos menn på 30 og 60 mg / kg / måned som representerer 1,2 og 2,2 ganger eksponeringsnivået ved maksimal anbefalt human dose på 150 mg. Disse svulstene kan være relatert til forlenget dopamin D2 -reseptorantagonisme og hyperprolaktinemi Relevansen av disse tumorfunnene hos gnagere når det gjelder risiko for mennesker er ukjent.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Polysorbat 20
Polyetylenglykol 4000
Sitronsyre monohydrat
Vannfritt di-natriumhydrogenfosfat
Natriumdihydrogenfosfatmonohydrat
Natriumhydroksid (for pH -justering)
Vann til injeksjonsvæsker
06.2 Uforlikelighet
Dette legemidlet må ikke blandes med andre legemidler.
06.3 Gyldighetsperiode
2 år.
06.4 Spesielle forholdsregler for lagring
Oppbevares ved en temperatur som ikke overstiger 30 ° C.
06.5 Emballasje og innhold i pakningen
Forfylt sprøyte (kopolymer med syklisk olefin) med stempelstopp, sprøytehåndtakvinger og låsekappe (brombutylgummi) med en sikkerhetsnål 22G, 0,72 mm x 38,1 mm og en sikkerhetsnål 23G, 1 tommer (0,64) mm x 25,4 mm).
Emballasje:
Pakningen inneholder 1 ferdigfylt sprøyte og 2 nåler
06.6 Bruksanvisning og håndtering
Ubrukte medisiner og avfall fra denne medisinen må kastes i henhold til lokale forskrifter
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
Janssen-Cilag International NV, Turnhoutseweg 30,
B-2340 Beerse, Belgia.
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
EU/1/11/672/004
041004045
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
04. mars 2011
10.0 DATO FOR REVISJON AV TEKSTEN
D.CCE mars 2015