Hva er Samsca?
Samsca er et legemiddel som inneholder virkestoffet tolvaptan. Den er tilgjengelig som blå tabletter (trekantet: 15 mg; runde: 30 mg).
Hva brukes Samsca til?
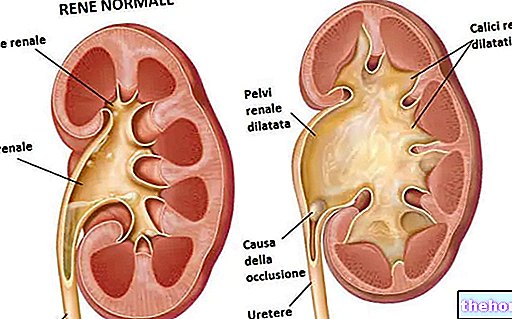
Samsca brukes til å behandle voksne med hyponatremi (eksepsjonelt lave nivåer av natrium i blodet) forårsaket av en tilstand som kalles "syndrom av upassende antidiuretisk hormonsekresjon" (SIADH). SIADH oppstår når det er for mye av et hormon som kalles "antidiuretisk hormon" eller "vasopressin", noe som reduserer urinproduksjonen ved å beholde vann i blodet. Dette resulterer i en fortynning av blodet og en påfølgende senking av natriumnivået.
Medisinen kan bare fås på resept.
Hvordan brukes Samsca?
Behandling med Samsca bør startes på sykehuset, slik at helsepersonell kan bestemme den mest passende dosen og overvåke pasientens blodnatriumnivå og blodvolum.
Startdosen er 15 mg en gang daglig. Det kan økes til maksimalt 60 mg en gang daglig for å oppnå et passende nivå av natrium og blodvolum. Tablettene skal svelges hele med et glass vann, og kan ikke tas med grapefruktjuice.
Hvordan fungerer Samsca?
Personer med SIADH inneholder en mengde vasopressin, noe som fører til en redusert urinproduksjon og en tynning av blodet. Den aktive ingrediensen i Samsca, tolvaptan, er en vasopressin 2. reseptorantagonist Dette betyr at den blokkerer en type reseptor (et protein) som vasopressin, et hormon, normalt fester seg til. Ved å blokkere denne reseptoren, Samsca, forhindrer vasopressin i å ha sin effekt. Dette fører til en økning i urinproduksjonen, reduserer mengden vann og øker nivået av natrium i blodet.
Hvordan har Samsca blitt studert?
Effekten av Samsca ble først testet i eksperimentelle modeller før den ble studert hos mennesker.
Samsca har blitt sammenlignet med placebo (en dummy -behandling) i to hovedstudier med 424 voksne med lave natriumnivåer forårsaket av SIADH og andre tilstander som lever- og hjerteproblemer. Hovedmålet for effektivitet var basert på endringen i
mengden natrium i blodet de første 30 dagene av behandlingen. Studien så også spesifikt på effekten av behandling i forskjellige sykdomsgrupper.
Hvilken fordel har Samsca vist under studiene?
Samsca var mer effektivt enn placebo for å øke natriumnivået i blodet ved alle sykdommer, men også hos SIADH -pasienter enn hos personer med lever- eller hjerteproblemer.
Natriumnivået var omtrent 129 mmol / l ved studiestart. Hos SIADH -pasienter økte nivåene med gjennomsnittlig 4,8 mmol / l på dag 4 hos de som ble behandlet med Samsca, sammenlignet med 0,2 mmol / l hos de som ble behandlet med placebo. På dag 30 hadde natrium økt med gjennomsnittlig 7,4 mmol / l hos pasienter som ble behandlet med Samsca, sammenlignet med 1,5 mmol / l hos pasienter som ble behandlet med placebo.
Hva er risikoen forbundet med Samsca?
Bivirkninger som oftest kan oppstå med Samsca (sett hos mer enn 1
pasient av 10) er tørste og kvalme. Den fullstendige listen over alle bivirkninger rapportert med Samsca, se pakningsvedlegget.
Samsca må ikke brukes til personer som kan være overfølsomme (allergiske) overfor tolvaptan eller noen av de andre ingrediensene. Det må ikke brukes til pasienter med anuri (manglende evne til å urinere), svært lavt blodvolum, lavt natriumnivå i blodet med begrensede blodvolumer, hypernatremi (overdrevent høyt natriumnivå i blodet) eller hos pasienter som ikke kan føle tørsten. Det bør også brukes til gravide eller ammende kvinner.
Hvorfor har Samsca blitt godkjent?
Komiteen for medisiner for mennesker (CHMP) bestemte at fordelene til Samsca er større enn risikoen for behandling av voksne pasienter med hyponatremi sekundært til SIADH. Komiteen anbefalte utstedelse av markedsføringstillatelse for Samsca.
Mer informasjon om Samsca:
3. august 2009 ga EU -kommisjonen Otuska Pharmaceutical Europe Ltd en "markedsføringstillatelse" for Samsca, gyldig i hele EU.
For hele versjonen av Samscas EPAR, klikk her.
Siste oppdatering av dette sammendraget: 06-2009.
Informasjonen om Samsca - tolvaptan som er publisert på denne siden kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.











-cos-cause-e-terapia.jpg)