Aktive ingredienser: Fingolimod
GILENYA 0,5 mg harde kapsler
Indikasjoner Hvorfor brukes Gilenya? Hva er den til?
Hva er Gilenya
Den aktive ingrediensen i Gilenya er fingolimod.
Hva Gilenya er til for
Gilenya brukes hos voksne for behandling av tilbakefall-remitterende multippel sklerose (MS), spesielt ved:
Pasienter som ikke har svart på terapi med MS -behandling.
eller
Pasienter med alvorlig utviklende alvorlig MS.
Gilenya kurerer ikke MS, men det bidrar til å redusere antall tilbakefall og bremse utviklingen av fysisk funksjonshemming forårsaket av MS.
Hva er multippel sklerose
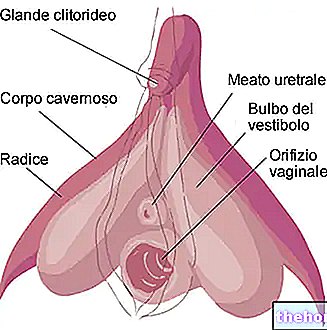
MS er en kronisk sykdom som påvirker sentralnervesystemet (CNS), som inkluderer hjernen og ryggmargen.Ved MS ødelegger betennelse den beskyttende kappen (kalt myelin) som linjer nervene i CNS og forhindrer nervene i å fungere som de burde. Denne prosessen kalles demyelinisering.
Tilbakefall-remitterende MS er preget av tilbakefallende angrep (tilbakefall) av nevrologiske symptomer som gjenspeiler en inflammatorisk tilstand i sentralnervesystemet. Symptomene varierer fra pasient til pasient, men innebærer vanligvis vanskeligheter med å gå, nummenhet, syn eller balanseforstyrrelser. Symptomene på tilbakefall kan forsvinne helt når tilbakefallet er over, men noen klager kan vedvare.
Hvordan Gilenya fungerer
Gilenya hjelper til med å beskytte nervesystemet mot angrep fra immunsystemet ved å redusere evnen til noen hvite blodlegemer (lymfocytter) til å sirkulere fritt i kroppen og forhindre at de når hjernen og ryggmargen. Dette begrenser nerveskaden forårsaket. Fra MS.
Kontraindikasjoner Når Gilenya ikke skal brukes
Ikke ta Gilenya
- hvis du har redusert immunrespons (på grunn av et immunsvikt syndrom, en sykdom eller medisiner som reduserer immunsystemet).
- hvis du har en alvorlig pågående infeksjon eller en kronisk pågående infeksjon som hepatitt eller tuberkulose.
- hvis du har aktiv kreft (bortsett fra hvis det er en type hudkreft som kalles basalcelle hudkreft).
- hvis du har alvorlige leverproblemer.
- dersom du er allergisk overfor fingolimod eller noen av de andre innholdsstoffene i dette legemidlet.
Informer legen din før du tar Gilenya hvis noen av disse gjelder deg.
Forholdsregler for bruk Hva du må vite før du bruker Gilenya
Snakk med legen din før du tar Gilenya:
- hvis du har uregelmessig, unormal hjerterytme.
- hvis du opplever symptomer på lav puls (f.eks. svimmelhet, kvalme eller hjertebank).
- hvis du har noen hjerteproblemer, blokkering av blodårene i hjertet ditt, tidligere har hatt hjerteinfarkt eller hjertestans eller har angina.
- hvis du har hatt et slag tidligere.
- hvis du lider av hjertesvikt.
- hvis du har alvorlige pusteproblemer mens du sover (alvorlig søvnapné).
- hvis du har blitt fortalt at du har en unormal EKG.
- hvis du tar eller nylig har tatt medisiner mot uregelmessig hjerterytme, for eksempel kinidin, disopyramid, amiodaron eller sotalol.
- hvis du tar eller nylig har tatt medisiner som reduserer hjerterytmen (for eksempel betablokkere, verapamil, diltiazem eller ivabradin, digoksin, antikolinesterasemedisiner eller pilokarpin).
- hvis du noen gang har hatt episoder med plutselig bevissthetstap eller besvimelse (synkope).
- hvis du har tenkt å bli vaksinert.
- hvis du aldri har hatt vannkopper.
- hvis du har eller har hatt synsforstyrrelser eller andre tegn på hevelse i det sentrale synsområdet (macula) på baksiden av øyet (en tilstand som kalles makulaødem, se nedenfor), hvis du har eller har hatt en "betennelse eller" infeksjon i øyet (uveitt), eller hvis du har diabetes (som kan forårsake øyeproblemer).
- hvis du har leverproblemer.
- hvis du har høyt blodtrykk som ikke kan kontrolleres av medisiner.
- hvis du har alvorlige lungeproblemer eller har hoste av røyking.
Informer legen din før du tar Gilenya hvis noen av disse gjelder deg.
Langsom hjertefrekvens (bradykardi) og uregelmessig hjerterytme: Ved starten av behandlingen forårsaker Gilenya pulsen redusert. Som et resultat kan du oppleve svimmelhet eller tretthet, bevissthet om hjerteslag eller blodtrykksfall. lege, da du kan trenge øyeblikkelig behandling. Gilenya kan også forårsake uregelmessig hjerterytme, spesielt etter den første dosen. Uregelmessig hjerterytme går vanligvis tilbake til det normale på mindre enn et døgn. Langsom puls går vanligvis tilbake. går tilbake til det normale innen en måned.
Legen din vil be deg om å bli på klinikken eller sykehuset i minst 6 timer etter administrering av den første dosen Gilenya, hvor pulsen og blodtrykket ditt måles når som helst: på denne måten kan passende tiltak iverksettes i tilfelle av bivirkninger som oppstår ved behandlingsstart Du må ha et elektrokardiogram tilgjengelig før den første dosen Gilenya og etter 6 timers overvåking. Legen din kan kontrollere elektrokardiogrammet kontinuerlig i løpet av denne perioden. Hvis etter 6 o ' timer. pulsen din er veldig lav eller synker, eller hvis EKG viser abnormiteter, må du kanskje observeres i en lengre periode (minst ytterligere 2 timer og muligens til neste morgen), til disse problemene er løst. det samme kan skje hvis hun tar G igjen ilenya etter avbrudd i behandlingen, avhengig av hvor lenge avbruddet var og hvor lenge du har tatt Gilenya før avbruddet.
Hvis du har eller er i fare for å få uregelmessig eller unormal hjerterytme, hvis EKG er unormalt, eller hvis du har hjertesykdom eller hjertesvikt, er det ikke sikkert at Gilenya passer for deg.
Hvis du noen gang har hatt episoder med plutselig bevissthetstap eller redusert hjertefrekvens, er det ikke sikkert at Gilenya passer for deg. Du vil bli sett av en kardiolog (hjertespesialist) som vil gi deg råd om hvordan du starter behandlingen med Gilenya, inkludert overvåking til neste morgen.
Hvis du tar medisiner som kan forårsake nedsatt hjertefrekvens, er det ikke sikkert at Gilenya passer for deg. Du vil bli sett av en kardiolog som vil vurdere om du kan ta medisiner som ikke reduserer pulsen din som et alternativ og lar deg starte behandling med Gilenya. Hvis denne endringen i terapi ikke er mulig, vil kardiologen gi deg råd om hvordan du starter behandlingen med Gilenya, inkludert overvåkning til neste morgen.
Hvis du aldri har hatt vannkopper: Hvis du aldri har hatt vannkopper, vil legen din kontrollere immuniteten din mot viruset som forårsaker det (varicella zoster -virus). Hvis du ikke er beskyttet mot viruset, kan du trenge vaksinasjon før du starter behandling med Gilenya. Hvis dette skjer, vil legen din utsette starten på Gilenya -behandlingen i opptil en måned etter fullført vaksinasjonskurs.
Infeksjoner: Gilenya reduserer antall hvite blodlegemer (spesielt lymfocytter). Hvite blodlegemer bekjemper infeksjoner. Når du tar Gilenya (og opptil 2 måneder etter avsluttet behandling), kan du lettere få infeksjoner. Enhver eksisterende infeksjon kan bli verre. Infeksjoner kan være alvorlige og livstruende. Hvis du tror du har en infeksjon, har feber, har influensasymptomer eller har hodepine ledsaget av stiv nakke, lysfølsomhet, kvalme og / eller forvirring (dette kan være symptomer på hjernehinnebetennelse) lege med en gang ..
Makulaødem: Før du starter behandling med Gilenya, hvis du har eller har hatt synsforstyrrelser eller andre tegn på hevelse i det sentrale synsområdet (macula) på baksiden av øyet, hvis du har eller har hatt et "betennelses- eller" infeksjonsøye (uveitt) eller hvis du har diabetes, kan legen din be deg om å få en øyeundersøkelse.
Legen din kan be deg om å få en øyeundersøkelse 3-4 måneder etter at du har startet behandlingen med Gilenya.
Makulaen er et lite område av netthinnen på baksiden av øyet som lar deg se former, farger og detaljer tydelig og skarpt. Gilenya kan forårsake hevelse i makulaen, en tilstand som er kjent som makulaødem. hevelse oppstår. vanligvis i de første 4 månedene av behandlingen med Gilenya.
Makulært ødem er mer sannsynlig hvis du har diabetes eller har hatt en "betennelse i øyet" kalt uveitt. I disse tilfellene vil legen din sjekke deg regelmessig for de første tegnene på makulaødem.
Snakk med legen din før du starter behandlingen med Gilenya hvis du har hatt makulaødem.
Makulaødem kan forårsake noen av de visuelle symptomene (optisk nevritt) som også oppstår under MS -angrep. I begynnelsen kan det være ingen symptomer. Sørg for å fortelle legen din om eventuelle synendringer. Legen din kan be deg om å henvise til dem . gjennomgå en øyeundersøkelse, spesielt hvis:
- det sentrale visningsområdet er ute av fokus eller har skygger;
- en blind flekk utvikler seg i det sentrale synsområdet;
- har problemer med å skille farger eller fine detaljer.
Leverfunksjonstester: Hvis du har alvorlige leverproblemer, bør du ikke ta Gilenya. Behandling med Gilenya kan påvirke leverfunksjonen din. Du vil sannsynligvis ikke legge merke til noen symptomer, men hvis du merker gulfarging av huden eller det hvite i øynene, unormal mørk urin eller uforklarlig kvalme og oppkast, fortell legen din umiddelbart.
Informer legen din umiddelbart hvis du får noen av disse symptomene etter at du har startet Gilenya -behandlingen.
I løpet av de første tolv månedene av behandlingen vil legen be deg om å ta blodprøver for å kontrollere leverfunksjonen din. Hvis resultatene indikerer at det er et leverproblem, kan det hende at behandlingen med Gilenya må stoppes.
Høytrykk
Fordi Gilenya forårsaker en liten økning i blodtrykket, kan legen din sjekke blodtrykket ditt regelmessig. Lungeproblemer Gilenya har en svak effekt på lungefunksjonen. Hos pasienter med alvorlige lungeproblemer eller hoste fra røyking, kan bivirkninger lettere oppstå.
Blodtall Ønsket effekt av behandling med Gilenya er å redusere mengden hvite blodlegemer i blodet. Disse går vanligvis tilbake til det normale innen 2 måneder etter at behandlingen er stoppet. Fortell legen din at du tar Gilenya hvis du må ta blodprøver. .
Før du starter behandlingen med Gilenya, vil legen din bekrefte om antallet hvite blodlegemer er tilstrekkelig, og kan be deg om å gjenta tellingen regelmessig. Hvis du ikke har nok hvite blodlegemer, må du kanskje slutte å ta Gilenya.
Posterior reversibel encefalopatisyndrom (PRES)
Et syndrom kalt posterior reversibel encefalopati (PRES) har blitt rapportert sjelden hos pasienter med multippel sklerose behandlet med Gilenya. Symptomer kan inkludere plutselig alvorlig hodepine, forvirring, anfall og endringer i synet. Fortell legen din dersom noen av disse symptomene oppstår under behandling med Gilenya.
Bruk hos eldre
Erfaring med Gilenya hos eldre pasienter over 65 år er begrenset. Spør legen din hvis du har ytterligere spørsmål.
Barn og ungdom
Gilenya er ikke beregnet på bruk hos barn og ungdom under 18 år siden det ikke er undersøkt hos MS -pasienter under 18 år.
Interaksjoner Hvilke medisiner eller matvarer kan endre effekten av Gilenya
Fortell legen din eller apoteket dersom du bruker, nylig har brukt eller planlegger å bruke andre legemidler. Fortell legen din dersom du tar noen av følgende medisiner:
- Legemidler som undertrykker eller endrer immunsystemet, inkludert andre legemidler som brukes til å behandle MS, for eksempel interferon beta, glatirameracetat, natalizumab, mitoksantron, teriflunomid, dimetylfumarat eller alemtuzumab. Du bør ikke bruke Gilenya med disse legemidlene, da de kan forsterke effekten på immunsystemet (se også "Bruk ikke Gilenya").
- Kortikosteroider, på grunn av mulig additiv effekt på immunsystemet.
- Vaksiner. Spør legen din om råd først hvis du trenger vaksinasjon. I løpet av og opptil 2 måneder etter behandling med Gilenya, bør du ikke motta noen typer vaksiner (levende svekkede vaksiner), da de kan utløse infeksjonen de skulle forhindre. Andre vaksiner fungerer kanskje ikke like bra som vanlig hvis de gis på dette tidspunktet ...
- Legemidler som senker hjerterytmen (for eksempel betablokkere, for eksempel atenolol). Samtidig bruk av Gilenya med disse legemidlene kan forsterke effekten på hjertefrekvensen de første dagene av Gilenya -behandlingen.
- Medisiner mot uregelmessig hjerterytme, for eksempel kinidin, disopyramid, amiodaron eller sotalol. Legen din kan beslutte å ikke foreskrive Gilenya hvis du tar denne typen medisiner, da de kan forsterke effekten på uregelmessig hjerterytme.
- Andre medisiner:
- proteasehemmere, anti-infeksjonsmidler som ketokonazol, azol-antifungale midler, klaritromycin eller telitromycin.
- karbamazepin, rifampicin, fenobarbital, fenytoin, efavirenz eller johannesurt (potensiell risiko for redusert effekt).
Advarsler Det er viktig å vite at:
Graviditet og amming
Før du starter behandlingen med Gilenya, kan legen be deg om å ta en graviditetstest for å sikre at du ikke er gravid. Mens du tar Gilenya eller i to måneder etter at behandlingen er avsluttet, bør du unngå å bli gravid, da det er fare for at barnet blir skadet. Snakk med legen din om pålitelige prevensjonsmetoder som skal brukes under behandlingen. Med Gilenya og i 2 måneder etter at behandlingen er avsluttet. .
Hvis du blir gravid mens du tar Gilenya, må du stoppe behandlingen og fortelle legen din umiddelbart. Legen din vil sammen med deg bestemme hva som er best for deg og babyen din.
Du må ikke amme mens du tar Gilenya. Gilenya utskilles i morsmelk med risiko for alvorlige bivirkninger for nyfødte.
Rådfør deg med lege eller apotek før du tar medisiner.
Kjøring og bruk av maskiner
Legen din vil fortelle deg om sykdommen din lar deg kjøre bil og bruke maskiner på en trygg måte. Gilenya forventes ikke å påvirke evnen til å kjøre bil og bruke maskiner.
Ved starten av behandlingen må du imidlertid bli på legekontoret eller sykehuset i 6 timer etter at du har tatt den første dosen Gilenya. Evnen til å kjøre bil og bruke maskiner kan være svekket i løpet av denne tiden og potensielt utover.
Dosering og bruksmåte Hvordan bruke Gilenya: Dosering
Behandling med Gilenya vil bli overvåket av en lege med erfaring i behandling av multippel sklerose.
Ta alltid dette legemidlet nøyaktig slik legen din har fortalt deg.
Rådfør deg med lege hvis du er i tvil. Dosen er en kapsel en gang daglig. Ta Gilenya en gang om dagen med et glass vann. Gilenya kan tas med eller uten mat.
Å ta Gilenya til samme tid hver dag vil hjelpe deg med å huske når du skal ta medisinen.
Ikke overskrid anbefalt dose.
Legen din kan bytte deg direkte fra behandling med interferon beta, glatirameracetat eller dimetylfumarat til Gilenya hvis det ikke er tegn på abnormiteter forårsaket av tidligere behandling. Legen din kan få deg til å ta en blodprøve for å utelukke disse abnormitetene. Etter å ha stoppet natalizumab kan det være nødvendig å vente 2-3 måneder før du starter behandling med Gilenya. For bytte fra teriflunomid kan legen din råde deg til å vente en viss tid eller fortsette med en akselerert eliminasjonsprosedyre. Hvis du har blitt behandlet med alemtuzumab, er det nødvendig med grundig evaluering og diskusjon med legen din for å avgjøre om Gilenya passer for deg.
Rådfør deg med lege eller apotek hvis du er usikker på hvor lenge du skal ta Gilenya.
Overdosering Hva du skal gjøre hvis du har tatt for mye Gilenya
Dersom du tar for mye av Gilenya
Fortell legen din umiddelbart hvis du har tatt for mange Gilenya kapsler.
Dersom du har glemt å ta Gilenya
Hvis du har tatt Gilenya i mindre enn 1 måned og glemmer å ta 1 dose for en hel dag, snakk med legen din før du tar neste dose. Legen din kan bestemme seg for å observere deg når du tar din neste dose.
Hvis du har tatt Gilenya i minst 1 måned og har glemt å ta medisinen i mer enn 2 uker, må du snakke med legen din før du tar neste dose. Legen din kan bestemme seg for å observere deg når du tar din neste dose. Hvis du imidlertid har glemt å ta medisinen i 2 uker eller mindre, kan du ta neste dose som planlagt.
Ta aldri en dobbel dose for å gjøre opp for en glemt dose.
Dersom du slutter å ta Gilenya
Ikke slutte å ta Gilenya eller endre dosen din uten å snakke med legen din først.
Gilenya vil forbli i kroppen i opptil 2 måneder etter at behandlingen er avsluttet. Antallet hvite blodlegemer (lymfocytter) kan forbli lavt i løpet av denne tiden, og bivirkningene som er beskrevet i dette pakningsvedlegget kan fortsatt forekomme. Etter å ha stoppet behandlingen med Gilenya kan det være nødvendig å vente 6-8 uker før du starter en ny behandling for multippel sklerose.
Hvis du trenger å starte Gilenya på nytt etter mer enn 2 ukers behandlingstopp, kan effekten på hjertefrekvensen som normalt oppstår ved behandlingsstart oppstå igjen. Sykehus under observasjon Ikke start Gilenya på nytt etter å ha stoppet det i mer enn to uker uten å konsultere din lege. doktor.
Spør lege eller apotek hvis du har ytterligere spørsmål om bruken av dette legemidlet
Bivirkninger Hva er bivirkningene av Gilenya
Som alle andre legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det.
Noen bivirkninger kan være eller bli alvorlige
Vanlige (kan forekomme hos opptil 1 av 10 personer):
- Hoste med slim, ubehag i brystet, feber (tegn på lungesykdommer)
- Herpesvirusinfeksjon (St. Anthony's fire eller herpes zoster), med symptomer som blemmer, svie, kløe eller smerter i huden, vanligvis i overkroppen eller i ansiktet. Andre symptomer kan være feber og svakhet i de tidlige stadiene . infeksjon, etterfulgt av nummenhet, kløe eller røde flekker med sterke smerter
- Langsom hjerterytme (bradykardi), uregelmessig hjerterytme
Mindre vanlige (kan forekomme hos opptil 1 av 100 personer):
- Lungebetennelse med symptomer som feber, hoste, pustevansker
- Makulaødem (hevelse i det sentrale synsområdet på netthinnen på baksiden av øyet) med symptomer som skygger eller blinde flekker i senteret, tåkesyn, problemer med å skille farger eller detaljer
Sjeldne (kan forekomme hos opptil 1 av 1000 personer):
- Et syndrom som kalles posterior reversibel encefalopati. Symptomer kan omfatte plutselig alvorlig hodepine, forvirring, anfall og / eller synsforstyrrelser
Isolerte tilfeller:
- Kryptokokkinfeksjoner (en type soppinfeksjon), inkludert kryptokokk -meningitt med symptomer som hodepine ledsaget av stivhet i nakken, lysfølsomhet, kvalme og / eller forvirring.
Fortell legen din umiddelbart hvis du får noen av disse bivirkningene.
Andre bivirkninger
Svært vanlige (kan forekomme hos flere enn 1 av 10 personer):
- Influensavirusinfeksjon med symptomer som tretthet, frysninger, ondt i halsen, ledd- eller muskelsmerter, feber
- Følelse av trykk eller smerter i kinnene og pannen (bihulebetennelse)
- Hodepine
- Diaré
- Ryggsmerte
- Blodprøver som viser høyere nivåer av leverenzymer
- Hoste
Vanlige (kan forekomme hos opptil 1 av 10 personer):
- Ringorm, en "soppinfeksjon i huden (pityriasis versicolor)
- Svimmelhet
- Alvorlig hodepine ofte ledsaget av kvalme, oppkast og lysfølsomhet (migrene)
- Lavt nivå av hvite blodlegemer (lymfocytter, leukocytter)
- Svakhet
- Hudutslett med kløe, rødhet og svie (eksem)
- Kløe
- Økte nivåer av fett (triglyserider) i blodet
- Hårtap
- Piping
- Depresjon
- Sløret syn (se også avsnittet om "makulaødem" Noen bivirkninger kan være eller bli alvorlige ")
- Hypertensjon (Gilenya kan forårsake en liten økning i blodtrykket)
Mindre vanlige (kan forekomme hos opptil 1 av 100 personer):
- Lavt nivå av noen hvite blodlegemer (nøytrofiler)
- Deprimert humør
Sjeldne (kan forekomme hos opptil 1 av 1000 personer):
- Blodkarforstyrrelser
- Lidelser i nervesystemet
- Kreft i lymfesystemet (lymfom)
Ikke kjent (frekvensen kan ikke estimeres ut fra tilgjengelige data):
- Allergisk reaksjon og hudutslett
Fortell legen din dersom noen av disse bivirkningene oppstår alvorlig.
Rapportering av bivirkninger
Rådfør deg med lege eller apotek dersom du får bivirkninger, inkludert mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget. Du kan også rapportere bivirkninger direkte via det nasjonale rapporteringssystemet som er oppført i vedlegg V. Ved å rapportere bivirkninger kan du hjelpe til med å gi mer informasjon om sikkerheten til dette legemidlet.
Utløp og oppbevaring
Hold denne medisinen utilgjengelig for barn.
Ikke bruk dette legemidlet etter utløpsdatoen som er angitt på esken og blisterpakningen etter "EXP" / "EXP". Utløpsdatoen refererer til den siste dagen i den måneden.
Oppbevares ved høyst 25 ° C.
Oppbevares i originalpakningen for å beskytte medisinen mot fuktighet.
Ikke bruk pakker som er skadet eller viser tegn på manipulering.
Ikke kast medisiner i avløpsvann eller husholdningsavfall. Spør apoteket om hvordan du skal kaste medisiner du ikke bruker lenger. Dette vil bidra til å beskytte miljøet.
Hva Gilenya inneholder
- Den aktive ingrediensen er fingolimod. Hver kapsel inneholder 0,5 mg fingolimod (som hydroklorid).
- Andre innholdsstoffer er: Kapselinnhold: magnesiumstearat, mannitol Kapselskall: gult jernoksid (E172), titandioksid (E171), gelatin Blekk: lakk (E904), dehydrert alkohol, isopropylalkohol, butylalkohol, propylenglykol, renset vann , konsentrert ammoniakkløsning, kaliumhydroksid, svart jernoksid (E172), gult jernoksid (E172), titandioksid (E171), dimetikon
Hvordan Gilenya ser ut og innholdet i pakningen
Gilenya 0,5 mg harde kapsler har en ugjennomsiktig hvit, ugjennomsiktig kropp og en dyp gul, ugjennomsiktig hette. Den svarte skriften "FTY0,5mg" er gravert på hodet og to gule bånd er gravert på kroppen.
Gilenya er tilgjengelig i pakninger som inneholder 7, 28 eller 98 kapsler, eller i flerpakninger som inneholder 84 kapsler (3 pakninger med 28 kapsler). Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
Kildepakningsvedlegg: AIFA (Italian Medicines Agency). Innhold publisert i januar 2016. Informasjonen som er tilstede er kanskje ikke oppdatert.
For å få tilgang til den mest oppdaterte versjonen, er det lurt å gå til nettstedet til AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttig informasjon.
01.0 LEGEMIDLETS NAVN
GILENYA 0,5 MG HARDE KAPSULER
▼ Legemiddel underlagt ytterligere overvåking. Dette vil tillate rask identifisering av ny sikkerhetsinformasjon. Helsepersonell oppfordres til å rapportere alle mistenkte bivirkninger. Se avsnitt 4.8 for informasjon om hvordan du rapporterer bivirkninger.
02.0 KVALITATIV OG KVANTITATIV SAMMENSETNING
Hver hard kapsel inneholder 0,5 mg fingolimod (som hydroklorid).
For fullstendig liste over hjelpestoffer, se pkt.6.1.
03.0 LEGEMIDDELFORM
Hard kapsel.
16 mm kapsel med intens gul ugjennomsiktig hette og hvit ugjennomsiktig kropp; svart gravering "FTY0.5 mg" på hodet og to sirkulære gule bånd gravert på kroppen.
04.0 KLINISK INFORMASJON
04.1 Terapeutiske indikasjoner
Gilenya er angitt alene, som et sykdomsmodifiserende legemiddel, i svært aktiv tilbakefall-remitterende multippel sklerose i følgende voksne pasientgrupper:
- Pasienter med høy sykdomsaktivitet til tross for behandling med minst én behandling sykdomsmodifiserende (se avsnitt 4.4 og 5.1 for unntak og informasjon om vask ut).
Disse pasientene kan defineres som de som ikke har svart på et fullstendig og tilstrekkelig behandlingsforløp (vanligvis minst ett års behandling) med minst én behandling sykdomsmodifiserende. Pasienter må ha hatt minst 1 tilbakefall det foregående året mens de var i behandling, og ha minst 9 T2 hyperintense lesjoner på hjernens MR eller minst 1 gadoliniumforsterkende lesjon. En pasient ikke-responderer det kan også defineres som en pasient som har en uendret eller økt tilbakefallshastighet sammenlignet med året før eller som har alvorlige tilbakefall.
eller
-Pasienter med raskt utviklende alvorlig tilbakefall-remitterende multippel sklerose, definert av to eller flere deaktiverende tilbakefall på ett år, og med 1 eller flere gadolinium-forsterkende lesjoner på hjernens MR eller med en betydelig økning i T2 lesjonsbelastning sammenlignet med en tidligere MR nylig utført.
04.2 Dosering og administrasjonsmåte
Behandlingen bør startes og overvåkes av en lege med erfaring i multippel sklerose.
Dosering
Den anbefalte dosen Gilenya er en 0,5 mg kapsel tatt oralt en gang daglig. Gilenya kan tas både under og fra måltider.
Det anbefales å utføre den samme overvåking som ved starten av behandlingen etter den første dosen hvis behandlingen stoppes for:
• 1 eller flere dager i løpet av de to første ukene av behandlingen
• mer enn 7 dager i løpet av tredje og fjerde behandlingsuke
• mer enn 2 uker etter en måneds behandling.
Hvis behandlingen er kortere enn beskrevet ovenfor, bør behandlingen fortsette med administrering av neste dose som planlagt (se pkt. 4.4).
Spesielle populasjoner
Pensjonister
Gilenya bør brukes med forsiktighet hos pasienter 65 år og eldre, da det ikke er tilstrekkelige data om sikkerhet og effekt tilgjengelig (se pkt. 5.2).
Nedsatt nyrefunksjon
I de viktigste sentrale studiene utført ved multippel sklerose har Gilenya ikke blitt studert hos pasienter med nedsatt nyrefunksjon. Basert på kliniske farmakologiske studier er det ikke nødvendig med dosejustering hos pasienter med lett til alvorlig nedsatt nyrefunksjon.
Nedsatt leverfunksjon
Gilenya må ikke brukes til pasienter med alvorlig nedsatt leverfunksjon (Child-Pugh klasse C) (se pkt. 4.3). Selv om det ikke er nødvendig med dosejustering hos pasienter med mild eller moderat nedsatt leverfunksjon, anbefales forsiktighet når behandling starter hos disse pasientene (se pkt. 4.4 og 5.2).
Diabetespasienter
Gilenya er ikke undersøkt hos pasienter med multippel sklerose og diabetes mellitus. Gilenya bør brukes med forsiktighet hos disse pasientene på grunn av en mulig økt risiko for makulaødem (se pkt.4.4 og 4.8). Disse pasientene bør gjennomgå regelmessige oftalmologiske undersøkelser for tegn på makulaødem.
Pediatrisk populasjon
Sikkerhet og effekt av Gilenya hos barn i alderen 0-18 år er ennå ikke fastslått.Tilgjengelige data er beskrevet i avsnitt 5.2, men ingen anbefalinger om dosering kan gis.
04.3 Kontraindikasjoner
- Diagnostisert immunsvikt syndrom.
- Pasienter som har økt risiko for opportunistiske infeksjoner, inkludert immunkompromitterte pasienter (inkludert de som er behandlet med samtidige immunsuppressive behandlinger eller de som er immunkompromitterte av tidligere behandlinger).
- Alvorlige aktive infeksjoner, kroniske aktive infeksjoner (hepatitt, tuberkulose).
- Diagnostiserte aktive ondartede svulster, med unntak av pasienter med basalcellekreft i huden.
- Alvorlig nedsatt leverfunksjon (Child-Pugh klasse C).
- Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene listet opp i pkt.6.1.
04.4 Spesielle advarsler og passende forholdsregler for bruk
Bradyarytmi
Oppstart av Gilenya -behandling resulterer i en forbigående reduksjon i hjertefrekvensen og kan også være forbundet med forsinkelser i atrioventrikulær ledning, inkludert isolerte episoder med fullstendig, forbigående og spontant oppløsende atrioventrikulær blokk (se pkt. 4.8 og 5.1).
Etter administrering av den første dosen begynner nedgangen i hjertefrekvensen innen en time og er maksimal i løpet av de første 6 timene. I de påfølgende dagene vedvarer denne etterdoseeffekten, selv om den vanligvis er av mindre intensitet, og reduseres vanligvis i løpet av de påfølgende ukene ... Ved fortsatt administrering går gjennomsnittlig hjertefrekvens tilbake til baseline innen en måned. Spesielt pasienter kan imidlertid være at pulsen ikke går tilbake til baseline innen slutten av den første måneden. Unormale konduksjoner har vanligvis vært forbigående og asymptomatiske. Vanligvis ikke nødvendig behandling og løste seg i løpet av de første 24 timene etter at behandlingen startet. Om nødvendig kan reduksjonen i hjertefrekvensen indusert av fingolimod reverseres ved parenteral administrering av doser av atropin eller isoprenalin.
Alle pasienter bør ha et elektrokardiogram og blodtrykksmåling før den første dosen Gilenya og etter 6 timer. Alle pasientene bør overvåkes i 6 timer for tegn og symptomer på bradykardi, med timepuls og blodtrykksmåling. Kontinuerlig (sanntid) EKG-overvåking anbefales i løpet av disse 6 timene.
Hvis symptomer på bradyarytmi oppstår etter administrering, bør passende kliniske pasienthåndteringsprosedyrer startes og overvåkingen fortsettes til symptomene er forsvunnet. Skulle en pasient kreve farmakologisk intervensjon under overvåking etter den første dosen, bør overvåking gjøres til neste morgen på sykehus og bør gjentas etter den andre dosen Gilenya.
Hvis hjertefrekvensen ved slutten av 6 timer er den laveste etter den første dosen (noe som tyder på at den maksimale farmakodynamiske effekten på hjertet ennå ikke er åpenbar), bør monitoreringen fortsette i minst 2 timer og til hjertet frekvensen øker igjen. Ytterligere overvåking er også nødvendig (minst til neste morgen og uansett til symptomene er løst) hvis pulsen etter 6 timer etter administrering av den første dosen er slag per minutt, eller hvis elektrokardiogram viser atrioventrikulær blokk ny debut eller høyere, eller hvis QTc -intervallet er ≥500 msek. Utbruddet av tredje graders atrioventrikulær blokk når som helst må også føre til en forlengelse av overvåking (minst til neste morgen).
På grunn av risikoen for alvorlige rytmeforstyrrelser, bør Gilenya ikke brukes til pasienter med andre graders Mobitz type II eller høyere atrioventrikulær blokk, hos pasienter med sykt sinus syndrom eller sino-atrial blokk, symptomatisk bradykardi eller tilbakevendende synkope, eller hos pasienter med betydelig QT -forlengelse (QTc> 470 msek (kvinner) eller> 450 msek (menn)).Siden signifikant bradykardi kan bli dårlig tolerert hos pasienter med kjent iskemisk hjertesykdom (inkludert angina pectoris), cerebrovaskulær sykdom, hjerteinfarkt, kongestiv hjertesvikt, historie med hjertestans, ukontrollert hypertensjon eller alvorlig søvnapné, bør Gilenya ikke brukes ved disse pasientene. Behandling med Gilenya bør bare vurderes hos disse pasientene hvis de forventede fordelene oppveier den potensielle risikoen; Hvis det er besluttet å starte behandlingen med Gilenya, bør en kardiolog konsulteres før behandlingen starter for å definere den mest passende overvåking. Overvåking anbefales minst til neste morgen for oppstart av behandlingen (se også pkt. 4.5).
Gilenya er ikke undersøkt hos pasienter med arytmier som krever behandling med klasse Ia (f.eks. Kinidin, disopyramid) eller klasse III (f.eks. Amiodaron, sotalol) antiarytmika. Klasse Ia og klasse III antiarytmika har vært assosiert med tilfeller av torsades de pointes hos pasienter med bradykardi. Siden oppstart av behandling med Gilenya resulterer i en reduksjon i hjertefrekvensen, bør Gilenya ikke brukes samtidig med disse legemidlene.
Erfaring med Gilenya hos pasienter på samtidig behandling med betablokkere, kalsiumkanalblokkere som forårsaker nedsatt hjertefrekvens (som verapamil, diltiazem eller ivabradin), eller med andre legemidler som kan redusere hjertefrekvensen (f.eks. Digoksin, antikolinesterasemedisiner eller pilokarpin) Siden oppstart av Gilenya -behandling også er forbundet med redusert hjertefrekvens (se også pkt. 4.8 Bradyarytmi), kan samtidig bruk av disse legemidlene ved oppstart av Gilenya -behandling være forbundet med alvorlig bradykardi og hjerteblokk. På grunn av de potensielle additive effektene på hjertefrekvensen, bør behandling med Gilenya ikke startes hos pasienter som får disse legemidlene (se også pkt. 4.5). Hos disse pasientene bør behandling med Gilenya bare vurderes hvis de forventede fordelene oppveier den potensielle risikoen. Hvis behandling med Gilenya vurderes, anbefales det at en kardiolog konsulteres før behandling starter for å vurdere å bytte til andre legemidler som ikke forårsaker nedsatt hjertefrekvens. Hvis det ikke er mulig å stoppe behandlingen med disse legemidlene, bør en kardiolog konsulteres for å definere tilstrekkelig overvåking ved behandlingsstart. Overvåking minst til neste morgen anbefales (se også pkt. 4.5).
Avhengig av varigheten av avbruddet og behandlingsvarigheten (tiden mellom behandlingsstart og seponering), kan effektene på hjertefrekvensen og atrioventrikulær ledning komme tilbake når behandlingen med Gilenya starter på nytt. Det anbefales å utføre den samme overvåking som ved starten av behandlingen etter den første dosen hvis behandlingen stoppes for:
• 1 eller flere dager i løpet av de to første ukene av behandlingen
• mer enn 7 dager i løpet av tredje og fjerde behandlingsuke
• mer enn 2 uker etter en måneds behandling.
Hvis behandlingen er kortere enn beskrevet ovenfor, bør behandlingen fortsette med administrering av neste dose som planlagt.
QT -intervall
I en grundig QT -intervallstudie utført med fingolimod -doser på 1,25 mg eller 2,5 mg, ved steady state (når den negative kronotrope effekten av fingolimod fremdeles var tilstede), forårsaket behandling med fingolimod forlenget dose. Korrigert QT -intervall (QTc), med øvre grense på 90% konfidensintervall ≤ 13,0 ms. Det ble ikke observert dose-respons eller eksponering-respons-korrelasjon mellom forlengelse av fingolimod og QTc-intervall, verken som en absolutt verdi eller som en endring fra baseline.
Den kliniske betydningen av disse funnene er ukjent. Ingen klinisk signifikant forlengelse av QT -intervallet ble observert i studier på pasienter med multippel sklerose, men pasienter med risiko for å utvikle QT -intervallforlengelse ble ikke inkludert i kliniske studier.
Legemidler som kan forlenge QTc -intervallet bør unngås hos pasienter med betydelige risikofaktorer, for eksempel hypokalemi eller medfødt forlengelse av QT -intervallet.
Infeksjoner
En relevant farmakodynamisk effekt av Gilenya er den doseavhengige reduksjonen i perifere lymfocyttall til 20-30% av baselineverdiene. Dette skyldes reversibel binding av lymfocytter i lymfoide vev (se pkt.5.1).
Et nylig fullstendig blodtall (dvs. tatt innen 6 måneder før eller etter avsluttet tidligere behandling) bør være tilgjengelig før behandling med Gilenya startes. Det anbefales også under behandlingen å evaluere blodtall periodisk etter 3 måneder og minst årlig deretter, og ved tegn på infeksjon. Absolutt lymfocyttall under 0,2x109 / l, hvis bekreftet, bør føre til seponering. gå tilbake til det normale, ettersom fingolimod ble avbrutt i kliniske studier på pasienter med absolutt lymfocyttall under 0,2x109 / l.
Behandlingsstart med Gilenya bør utsettes hos pasienter med pågående alvorlige infeksjoner til restitusjon.
Pasienter bør evalueres for deres immunitetsstatus for vannkopper før behandling med Gilenya startes. I mangel av en lege-bekreftet historie med vannkopper eller bevis på et fullstendig varicella-vaksinasjonskurs, anbefales det at pasienter testes for antistoffer mot varicella-zoster-virus (VZV) før behandling med Gilenya startes. For pasienter med et negativt antistoff titer, anbefales et komplett vaksinasjonskurs mot varicella før behandling med Gilenya startes (se pkt. 4.8). Starten av behandlingen med Gilenya bør utsettes med 1 måned for at vaksinasjonen skal være fullstendig effektiv.
Virkningene av Gilenya på immunsystemet kan øke risikoen for infeksjoner (se pkt. 4.8). Effektive diagnostiske og terapeutiske strategier bør implementeres hos pasienter behandlet med Gilenya som har symptomer på infeksjoner. Pasienter bør instrueres til å rapportere symptomer på infeksjon til legen sin under behandling med Gilenya.
Hvis en alvorlig infeksjon utvikler seg hos en pasient, bør seponering av Gilenya-behandling vurderes, og nytte-risiko-balansen bør vurderes før behandlingen gjenopptas.
Eliminering av fingolimod etter seponering av behandlingen kan ta opptil to måneder, og infeksjonskontroll bør derfor fortsette i løpet av denne perioden. Pasienter bør instrueres i å rapportere symptomer på infeksjon innen to måneder etter at fingolimod er stoppet.
Makulært ødem
Makulaødem med eller uten synsforstyrrelser er rapportert hos 0,5% av pasientene som ble behandlet med 0,5 mg fingolimod, hovedsakelig i de første 3-4 månedene av behandlingen (se pkt. 4.8). En øyeundersøkelse anbefales derfor 3-4 måneder etter behandlingsstart.Hvis pasienter rapporterer synsforstyrrelser når som helst under behandlingen, bør en fundusundersøkelse, inkludert makula, utføres.
Pasienter med tidligere uveitt og pasienter med diabetes mellitus har økt risiko for å utvikle makulaødem (se pkt. 4.8). Gilenya er ikke undersøkt hos pasienter med multippel sklerose og samtidig diabetes mellitus. Det anbefales at pasienter med multippel sklerose og samtidig diabetes mellitus eller med uveitt tidligere gjennomgår en oftalmologisk vurdering før behandling starter og kontroller under behandlingen.
Fortsettelse av Gilenya -behandling hos pasienter med makulaødem er ikke undersøkt. Det anbefales at behandlingen med Gilenya avsluttes hvis det oppstår makulaødem hos en pasient. Når du skal avgjøre om behandlingen med Gilenya skal gjenopptas eller ikke, bør potensielle fordeler og risiko for den enkelte pasienten vurderes.
Leverfunksjon
Forhøyelser av leverenzymer, spesielt alaninaminotransferase (ALT), men også gammaglutamyltranspeptidase (GGT) og aspartattransaminase (AST) er rapportert hos pasienter med multippel sklerose behandlet med Gilenya. I kliniske studier forekom ALAT -forhøyelser ≥3 ganger øvre grense for normalområdet (ULN) hos 8,0% av pasientene som ble behandlet med fingolimod 0,5 mg sammenlignet med 1,9% av pasientene som ble behandlet med placebo .. Økninger med 5 ganger øvre grense for normalområdet forekom hos 1,8% av pasientene som ble behandlet med fingolimod og hos 0,9% av pasientene som ble behandlet med placebo.I kliniske studier ble behandlingen med fingolimod avbrutt hvis økningen var> 5 ganger øvre grense for normalområdet. Hos noen pasienter som ble behandlet på nytt etter seponering, oppsto hepatiske transaminasehevinger igjen, noe som bekreftet en sammenheng mellom denne økningen og stoffet. I kliniske studier forekom økninger i levertransaminaser når som helst under behandlingen, selv om de fleste skjedde i de første 12 månedene. Blodtransaminase -nivåene gikk tilbake til det normale ca. 2 måneder etter seponering av fingolimod.
Gilenya er ikke undersøkt hos pasienter med eksisterende alvorlig nedsatt leverfunksjon (Child-Pugh klasse C) og bør derfor ikke brukes til disse pasientene (se pkt. 4.3).
På grunn av de immunsuppressive egenskapene til fingolimod, bør oppstart av behandlingen forsinkes hos pasienter med aktiv viral hepatitt til oppløsningen av den aktive fasen.
Nylige analyser (dvs. i løpet av de foregående 6 månedene) av transaminase- og bilirubinnivåer bør være tilgjengelige før behandling påbegynnes med Gilenya. I fravær av kliniske symptomer, bør levertransaminase -nivåer kontrolleres etter 1, 3, 6, 9 og 12 måneder behandling og periodisk deretter. Hvis levertransaminase -nivåer når verdier som er større enn 5 ganger grensen for normal (ULN), bør det arrangeres hyppigere kontroller, inkludert kontroller for serumbilirubin og alkalisk fosfatase (ALP) Hvis etter gjentatte kontroller leveren transaminaseverdier forblir mer enn 5 ganger grensen for normal (ULN), bør behandlingen med Gilenya stoppes og startes på nytt bare når levertransaminaseverdiene er tilbake til det normale.
Hos pasienter som viser symptomer på nedsatt leverfunksjon, som uforklarlig kvalme, oppkast, magesmerter, tretthet, anoreksi, gulsott og / eller mørk urin, bør leverenzymnivåer evalueres; hvis signifikant leverskade er bekreftet (f.eks. levertransaminase -nivåer som overskrider den øvre grensen for normalområdet med mer enn 5 ganger og / eller økning i bilirubinnivået i serum), bør behandlingen med Gilenya seponeres.Gjenopptak av behandling vil avhenge av om en annen årsak til leverskade er identifisert eller ikke, og pasientens fordel ved å gjenoppta behandlingen kontra risikoen for leverdysfunksjon som gjentar seg.
Selv om det ikke finnes data som viser at pasienter med eksisterende leversykdom har økt risiko for å utvikle forhøyede leverfunksjonstester, bør det utvises forsiktighet ved administrering av Gilenya til pasienter med en historie med betydelig leversykdom.
Interferens med serologiske analyser
Ettersom fingolimod reduserer antallet lymfocytter i blodet ved omfordeling til sekundære lymfoide organer, kan det ikke brukes til å vurdere lymfocyttstatusen til en pasient behandlet med Gilenya. Laboratorietester som involverer bruk av sirkulerende mononukleære celler krever høyere blodvolumer på grunn av reduksjon i antall sirkulerende lymfocytter.
Effekter på blodtrykket
Pasienter med ikke-medisinsk kontrollert hypertensjon ble ekskludert fra kliniske forsøk med Gilenya før markedsføring; Derfor anbefales spesiell oppmerksomhet hvis pasienter med ukontrollert hypertensjon behandles med Gilenya.
I kliniske studier med pasienter med multippel sklerose var behandling med fingolimod 0,5 mg assosiert med en gjennomsnittlig økning på omtrent 3 mmHg i systolisk blodtrykk og ca. 1 mmHg diastolisk blodtrykk: disse økningene skjedde omtrent 1 måned senere. Behandlingsstart og fortsatte med Fortsatt behandling.I en toårig placebokontrollert studie ble hypertensjon rapportert som en bivirkning hos 6,5% av pasientene som ble behandlet med Gilenya 0,5 mg og hos 3,3% av pasientene som ble behandlet med placebo. Derfor bør blodtrykket ditt kontrolleres regelmessig under behandling med Gilenya.
Virkninger på luftveiene
Lette doseavhengige reduksjoner i tvunget ekspiratorisk volum (FEV1) og diffusjonskapasitet for karbonmonoksid (Dlco) ble observert under behandling med Gilenya, reduksjoner som skjedde den første måneden og forble stabile i løpet av behandlingen. Gilenya bør brukes med forsiktighet hos pasienter med alvorlige respiratoriske lidelser, lungefibrose og kronisk obstruktiv lungesykdom (se pkt. 4.8).
Posterior reversibel encefalopati syndrom
Sjeldne tilfeller av posterior reversibel encefalopati syndrom (PRES) har blitt rapportert i kliniske studier og etter markedsføring med 0,5 mg dose (se pkt. 4.8) Symptomer rapportert inkluderer plutselig alvorlig hodepine, kvalme, oppkast, endret mental status, visuell forstyrrelser og anfall. Symptomer på PRES er vanligvis reversible, men kan utvikle seg til iskemisk hjerneslag eller hjerneblødning. Forsinkelse i diagnose og behandling kan føre til permanente nevrologiske konsekvenser. Ved mistanke om PRES bør behandling med Gilenya avbrytes.
Tidligere behandling med immunsuppressive eller immunmodulerende behandlinger
Det er ikke utført studier for å evaluere effekten og sikkerheten til Gilenya når pasienter bytter fra teriflunomid, dimetylfumarat eller alemtuzumab til Gilenya Når pasienter bytter fra annen behandling. sykdomsmodifiserende i Gilenya må halveringstiden og virkningsmekanismen for den andre terapien tas i betraktning for å unngå en additiv effekt på immunsystemet og samtidig minimere risikoen for reaktivering av sykdommen. Det anbefales å evaluere et fullstendig blodtall før du starter behandling med Gilenya for å sikre at effektene på immunsystemet forårsaket av tidligere behandling (f.eks. cytopeni) har løst seg.
Gilenya -behandling kan generelt settes i gang umiddelbart etter avsluttet behandling med interferon eller glatirameracetat.
Når det gjelder dimetylfumarat, er perioden på vask ut Det må være tilstrekkelig å gjenopprette tilstrekkelige blodtall før behandling med Gilenya startes.
På grunn av natalizumabs lange halveringstid tar eliminering vanligvis opptil 2-3 måneder etter at behandlingen er avsluttet. Teriflumonid elimineres også sakte fra plasma. Uten en akselerert eliminasjonsprosedyre kan clearance av teriflunomid fra plasma ta fra flere måneder til 2 år. Det anbefales å utføre en akselerert eliminasjonsprosedyre som beskrevet i sammendraget av produktkarakteristika for teriflunomid, eller alternativt bør utvaskingsperioden ikke være mindre enn 3,5 måneder. Forsiktighet bør utvises når pasienter byttes fra natalizumab eller teriflunomidbehandling til Gilenya angående potensielle samtidige effekter på immunsystemet.
Alemtuzumab har intense og langvarige immunsuppressive effekter. Ettersom den virkelige varigheten av disse effektene er ukjent, anbefales det å ikke starte behandling med Gilenya etter alemtuzumab med mindre fordelene med behandling for den enkelte pasienten klart oppveier risikoen.
Beslutningen om å administrere langvarige kortikosteroidbehandlinger må tas etter nøye vurdering.
Samtidig administrering med potente CYP450 -induktorer
Fingolimod bør brukes med forsiktighet i kombinasjon med kraftige CYP450 -induktorer. Det anbefales ikke å administrere johannesurt samtidig (se pkt. 4.5).
Avbryt behandling
Basert på halveringstiden for legemidlet, hvis det tas en beslutning om å avbryte behandlingen med Gilenya, bør det være et intervall på 6 uker uten terapi slik at fingolimod kan tømmes fra blodet (se pkt.5.2) Lymfocyttene teller gradvis går tilbake til normale verdier innen 1-2 måneder etter avsluttet behandling (se pkt.5.1). Å starte andre behandlinger i løpet av dette tidsintervallet resulterer i samtidig eksponering for fingolimod. Bruk av immunsuppressive legemidler kort tid etter seponering av Gilenya -administrasjonen kan ha en ytterligere effekt på immunsystemet, og derfor anbefales forsiktighet.
04.5 Interaksjoner med andre legemidler og andre former for interaksjon
Antineoplastiske, immunmodulerende eller immunsuppressive behandlinger
Antineoplastiske, immunmodulerende eller immunsuppressive behandlinger bør ikke gis samtidig på grunn av risikoen for additive effekter på immunsystemet (se pkt. 4.3 og 4.4).
Forsiktighet bør også utvises når pasienter starter Gilenya-behandling etter avsluttet behandling med langtidsvirkende behandlinger med virkninger på immunsystemet, for eksempel natalizumab eller mitoksantron (se pkt. 4.4). av kortikosteroider var ikke assosiert med en økt infeksjonshastighet.
Vaksinasjoner
Vaksinasjoner kan være mindre effektive under behandlingen og opptil to måneder etter at behandlingen med Gilenya er avsluttet. Bruk av levende svekkede vaksiner kan utgjøre en risiko for infeksjoner og bør derfor unngås (se pkt. 4.4 og 4.8).
Stoffer som induserer bradykardi
Fingolimod ble studert i kombinasjon med atenolol og diltiazem. Når fingolimod ble administrert med atenolol i en interaksjonsstudie hos friske frivillige, var det ytterligere 15% reduksjon i hjertefrekvens ved oppstart av behandlingen; denne effekten ble ikke observert med diltiazem. På grunn av den potensielle additive effekten. Hjertefrekvens, bør Gilenya -behandling ikke startes hos pasienter som tar betablokkere eller andre legemidler som kan redusere hjertefrekvensen, for eksempel klasse Ia og III antiarytmika, kalsiumkanalblokkere (som ivabradin, verapamil eller diltiazem), digoksin, antikolinesteraser eller pilocarpine (se pkt.4.4 og 4.8 Hvis behandling med Gilenya vurderes for disse pasientene, bør en kardiolog konsulteres for å vurdere å bytte til andre legemidler som ikke forårsaker nedsatt hjertefrekvens eller definere tilstrekkelig overvåking ved behandlingsstart. Hvis det ikke er mulig å stoppe behandlingen med legemidler som reduserer hjertefrekvensen, anbefales det å overvåke minst til neste morgen.
Endringer i farmakokinetikken til fingolimod indusert av andre stoffer
Fingolimod metaboliseres hovedsakelig av CYP4F2. Andre enzymer som CYP3A4 kan også være involvert i metaboliseringen, spesielt ved kraftig induksjon av CYP3A4. Det forventes ikke at potensielle bærerproteinhemmere påvirker oppførselen til fingolimod. Samtidig administrering av fingolimod og ketokonazol resulterte i en 1,7 ganger økning i eksponering (AUC) for fingolimod og fingolimodfosfat via inhibering av CYP4F2. Forsiktighet bør utvises ved administrering av fingolimod med stoffer som kan hemme CYP3A4 (proteasehemmere, azol antifungale midler, noen makrolider som klaritromycin eller telitromycin).
Samtidig administrering av karbamazepin 600 mg to ganger daglig, nådde steady state, og en enkelt dose fingolimod 2 mg reduserte AUC for fingolimod og dets metabolitt med omtrent 40%Andre potente induktorer av CYP3A4 -enzymet, som rifampicin, fenobarbital, fenytoin, efavirenz og johannesurt, kan forårsake en reduksjon i AUC for fingolimod og metabolitten med minst denne størrelsen. Siden dette potensielt kan svekke effekten, bør det utvises forsiktighet ved administrering i kombinasjon. Samtidig administrering med johannesurt anbefales imidlertid ikke (se pkt. 4.4).
Endringer i farmakologi for andre stoffer indusert av fingolimod
Det er usannsynlig at Fingolimod interagerer med stoffer som hovedsakelig metaboliseres av CYP450 -enzymer eller substrater av viktige bærerproteiner.
Samtidig administrering av fingolimod og cyklosporin resulterte ikke i noen endring i eksponering for cyklosporin eller fingolimod, derfor forventes det ikke at fingolimod vil endre farmakokinetikken til legemidler som er substrater for CYP3A4.
Samtidig administrering av fingolimod med orale prevensjonsmidler (etinyløstradiol og levonorgestrel) resulterte ikke i noen endring i eksponering for oral prevensjon. Eksponering for slike legemidler.
04.6 Graviditet og amming
Kvinner i fertil alder / prevensjon hos kvinner
Før behandling med Gilenya påbegynnes, bør kvinner i fertil alder informeres om mulige alvorlige farer for fosteret og om behovet for å bruke effektive prevensjonsmidler under behandling med Gilenya. Siden det tar omtrent to måneder etter at behandlingen er avsluttet for å fjerne fingolimod fra kroppen (se pkt. 4.4), kan den potensielle risikoen for fosteret eksistere, og derfor må prevensjonstiltak fortsette i løpet av denne tiden.
Svangerskap
En negativ graviditetstest må være tilgjengelig før behandling påbegynnes hos kvinner i fertil alder.Kvinner bør ikke bli gravide under behandlingen, og effektiv prevensjon anbefales. Hvis en kvinne blir gravid mens hun tar Gilenya, anbefales det å avbryte behandlingen.
Dyrestudier har vist reproduksjonstoksisitet, inkludert fostertap og organskader, spesielt vedvarende arteriell stamme og ventrikelseptumdefekt (se pkt. 5.3) Videre er reseptoren som fingolimod virker på (sfingosin 1-fosfat) involvert i vaskulær dannelse under embryogenese. Det er svært begrensede data fra bruk av fingolimod hos gravide kvinner.
Det er ingen data om effekten av fingolimod på fødsel og fødsel.
Foringstid
Fingolimod utskilles i melk hos ammende dyr i konsentrasjoner 2-3 ganger høyere enn de som finnes i mors plasma (se pkt. 5.3) På grunn av potensialet for alvorlige bivirkninger av fingolimod hos spedbarn som ammes, bør kvinner i behandling med Gilenya ikke amme.
Fruktbarhet
Data fra prekliniske studier indikerer ikke at fingolimod er forbundet med økt risiko for nedsatt fruktbarhet (se pkt. 5.3).
04.7 Påvirkning av evnen til å kjøre bil og bruke maskiner
Gilenya har ingen eller ubetydelig påvirkning på evnen til å kjøre bil eller bruke maskiner.
Noen ganger kan det imidlertid oppstå svimmelhet eller søvnighet ved oppstart av behandling med Gilenya Det anbefales at pasienter observeres i 6 timer når behandling med Gilenya starter (se pkt. 4.4 Bradyarytmi).
04.8 Bivirkninger
Oppsummering av sikkerhetsprofilen
Sikkerhetspopulasjonen til Gilenya er avledet fra to fase III placebokontrollerte kliniske studier og en aktiv kontrollert fase III klinisk studie utført på pasienter med tilbakefall-remitterende multippel sklerose. Det inkluderer totalt 2.431 pasienter behandlet med Gilenya (0,5 eller 1,25 mg). I den 2-årige placebokontrollerte kliniske studien D2301 (FREEDOMS) ble 854 pasienter (placebo: 418 pasienter) behandlet med fingolimod. I den 2-årige, placebokontrollerte studien D2309 (FREEDOMS II) ble 728 pasienter med multippel sklerose (placebo: 355 pasienter) behandlet med fingolimod. Sammenslåtte resultater fra disse to studiene indikerer at de mest alvorlige bivirkningene som oppstod med Gilenya 0,5 mg var infeksjoner, makulaødem og forbigående atrioventrikulær blokk ved behandlingsstart De hyppigste bivirkningene (forekomst ≥ 10%) som forekom med Gilenya 0,5 mg var influensa, bihulebetennelse, hodepine, diaré, ryggsmerter, forhøyede leverenzymer og hoste. Den hyppigste bivirkningen med Gilenya 0,5 mg som førte til "seponering av behandlingen var" økte ALAT-nivåer i blodet (2,2%). I 1-års studie D2302 (TRANSFORMS) som involverte 849 pasienter behandlet med fingolimod og som brukte interferon beta-1α som kontroll, bivirkningene som oppsto var generelt lik de i de placebokontrollerte studiene, tatt i betraktning den forskjellige studiens varighet.
Bivirkninger rapportert for Gilenya 0,5 mg i studiene D2301 (FREEDOMS) og D2309 (FREEDOMS II) er listet opp nedenfor. Frekvenskategorier er definert ved bruk av følgende konvensjon: svært vanlig (≥ 1/10); vanlig (≥1 / 100,
Sammendragstabell over bivirkninger
* Ikke rapportert i FREEDOMS, FREEDOMS II og TRANSFORMS studier. Kategorisering av hendelsesfrekvens var basert på en estimert "fingolimod -eksponering av omtrent 10 000 pasienter i alle kliniske studier."
Beskrivelse av noen spesifikke bivirkninger
Infeksjoner
I kliniske studier med pasienter med multippel sklerose var den totale infeksjonshastigheten (65,1%) rapportert med dosen på 0,5 mg lik den som ble sett med placebo. Imidlertid var nedre luftveisinfeksjoner, hovedsakelig bronkitt og, i mindre grad, herpesinfeksjoner og lungebetennelse hyppigere hos pasienter behandlet med Gilenya.
Noen få tilfeller av spredt herpetisk infeksjon, inkludert dødelige tilfeller, har blitt rapportert selv med dosen på 0,5 mg.
Makulært ødem
I kliniske studier med pasienter med multippel sklerose forekom det makulaødem hos 0,5% av pasientene som ble behandlet med anbefalt dose på 0,5 mg og hos 1,1% av pasientene som ble behandlet med den høyere dosen (1, 25 mg). De fleste tilfellene forekom i løpet av de første 3-4 månedene av behandlingen. Noen pasienter rapporterte tåkesyn og redusert synsstyrke, andre var asymptomatiske og diagnosen ble stilt under et rutinemessig oftalmologisk besøk. Makulært ødem forbedret eller løste seg spontant etter avsluttet behandling Risikoen for tilbakefall etter re-eksponering for behandling er ikke undersøkt .
Forekomsten av makulaødem er økt hos pasienter med multippel sklerose med uveitt (17% med uveitt tidligere enn 0,6% uten uveitt). Gilenya er ikke undersøkt hos pasienter med multippel sklerose og diabetes mellitus. sykdom assosiert med økt risiko for makulaødem (se pkt. 4.4) I kliniske studier med nyretransplanterte pasienter, inkludert pasienter med diabetes mellitus, resulterte behandling med fingolimod 2,5 mg og 5 mg i økt dobbel forekomst av makulaødem.
Bradyarytmi
Start av behandling med Gilenya resulterer i en forbigående reduksjon i hjertefrekvensen og kan også være forbundet med forsinkelser i atrioventrikulær ledning. I kliniske studier på pasienter med multippel sklerose ble maksimal reduksjon i hjertefrekvens observert i løpet av de første 6 timene etter operasjonen. " initiering av behandlingen, med reduksjon i frekvens med gjennomsnittlig 12-13 slag per minutt under behandling med Gilenya 0,5 mg. En nedgang i hjertefrekvensen under 40 slag per minutt har blitt observert sjelden hos pasienter behandlet med Gilenya 0,5 mg. Gjennomsnittlig puls gikk tilbake til baseline innen 1 måned etter fortsatt behandling. Bradykardi var generelt asymptomatisk, men noen pasienter opplevde milde til moderate symptomer, inkludert hypotensjon, svimmelhet, tretthet og / eller hjertebank, som forsvant i løpet av de første 24 timene etter behandlingsstart (se også pkt. 4.4 og 5.1.).
I kliniske studier med pasienter med multippel sklerose ble første graders atrioventrikulær blokk (forlengelse av "PR-intervallet til EKG") observert hos 4,7% av pasientene som ble behandlet med fingolimod 0,5 mg, hos 2,8% av pasientene. Pasienter behandlet med intramuskulært interferon beta- 1α og hos 1,6% av pasientene behandlet med placebo. Andre grad atrioventrikulær blokk er rapportert hos mindre enn 0,2% av pasientene som ble behandlet med Gilenya 0,5 mg. Etter markedsføring er det rapportert om isolerte episoder av forbigående, spontant oppløsende fullstendig atrioventrikulær blokk i løpet av 6-timers overvåkingsperioden etter den første dosen Gilenya. Etter markedsføring var vanligvis forbigående, asymptomatisk og løst i løpet av de første 24 Selv om det ikke var nødvendig med medisinsk inngrep for de fleste pasientene, fikk en pasient som ble behandlet med Gilenya 0, 5 mg isoprenalin etter en asymptomatisk andregrads Mobitz type 1 atrioventrikulær blokk.
Etter markedsføring har isolerte hendelser med sen debut, inkludert forbigående asystol og uforklarlig død, skjedd innen 24 timer etter administrering av den første dosen. Evaluering av disse tilfellene kompliseres av tilstedeværelse av samtidige medisiner og / eller eksisterende tilstander Korrelasjonen mellom disse hendelsene med Gilenya er usikker.
Blodtrykk
I kliniske studier med pasienter med multippel sklerose var behandling med Gilenya 0,5 mg assosiert med en gjennomsnittlig økning i systolisk blodtrykk på omtrent 3 mmHg og diastolisk blodtrykk på omtrent 1 mmHg: disse økningene skjedde omtrent 1 måned senere. Behandlingsstart og opprettholdes med hypertensjon ble rapportert hos 6,5% av pasientene som ble behandlet med fingolimod 0,5 mg og hos 3,3% av pasientene som ble behandlet med placebo. første behandlingsdag (se også pkt.4.4 Påvirkning av blodtrykk).
Leverfunksjon
Forhøyelser av leverenzymer er rapportert hos pasienter med multippel sklerose behandlet med Gilenya. I kliniske studier ble asymptomatisk forhøyelse av ALAT-nivåer i blod ≥3 ganger og ≥5 ganger øvre grense for normalområdet (ULN) observert hos henholdsvis 8,0% og 1,8% av pasientene som ble behandlet med Gilenya. 0,5 mg. behandling etter seponering oppstod forhøyede levertransaminaser igjen, noe som bekreftet en sammenheng mellom denne økningen og legemidlet.I kliniske studier forekom forhøyninger i levertransaminaser når som helst under behandlingen, selv om de fleste skjedde i løpet av de første 12 månedene.ALAT -nivåene gikk tilbake til det normale ca. 2 måneder etter avsluttet behandling med Gilenya. Hos et lite antall pasienter (N = 10 ved dosen 1,25 mg, N = 2 ved dosen 0,5 mg), som opplevde ALAT -forhøyelser ≥5 ganger øvre grense for normalområdet og som fortsatte behandlingen med Gilenya, ALAT -verdier tilbake til det normale innen omtrent 5 måneder (se også pkt. 4.4 Leverfunksjon).
Nervesystemet lidelser
I kliniske studier har sjeldne hendelser som involverer nervesystemet, inkludert iskemisk og hemoragisk slag og atypiske nevrologiske lidelser, for eksempel hendelser som ligner på akutt disseminert encefalomyelitt (EAD).
Vaskulære patologier
Sjeldne tilfeller av perifer arteriell sykdom har forekommet hos pasienter behandlet med fingolimod ved høyere doser (1,25 mg).
Luftveiene
Lette doseavhengige reduksjoner i tvunget ekspiratorisk volum (FEV1) og diffusjonskapasitet for karbonmonoksid (Dlco) ble observert under behandling med Gilenya, reduksjoner som skjedde den første måneden og forble stabile i løpet av behandlingen. Ved måned 24 var den prosentvise reduksjonen fra grunnlinjen i forutsagt FEV1 2,7% for fingolimod 0,5 mg og 1,2% for placebo, en forskjell som forsvant etter at behandlingen ble stoppet. Dlco -reduksjonene i måned 24 var 3,3% for fingolimod 0,5 mg og 2,7% for placebo.
Lymfomer
Tilfeller av ulike typer lymfom har blitt rapportert både i kliniske studier og etter markedsføring, inkludert et dødelig tilfelle av Epstein-Barr-virus (EBV) positivt B-cellelymfom. Forekomst av lymfom-tilfeller (B-celle og T-celle ) var høyere i kliniske studier enn forventet i befolkningen generelt.
Hemofagocytisk syndrom
Svært sjeldne tilfeller av hemofagocytisk syndrom er rapportert (Hemofagocytisk syndrom, HPS) med dødelig utgang hos pasienter behandlet med fingolimod i forbindelse med en "infeksjon." HPS er en sjelden tilstand som er beskrevet i forbindelse med infeksjoner, immunsuppresjon og en rekke autoimmune sykdommer.
Rapportering av mistenkte bivirkninger
Rapportering av mistenkte bivirkninger som oppstår etter godkjenning av legemidlet er viktig, da det muliggjør kontinuerlig overvåking av nytte / risiko -balansen for legemidlet Helsepersonell bes rapportere alle mistenkte bivirkninger via det nasjonale rapporteringssystemet. I "Vedlegg V .
04.9 Overdosering
Enkeltdoser opptil 80 ganger anbefalt dose (0,5 mg) ble godt tolerert hos friske frivillige. Ved dosen på 40 mg rapporterte 5 av de 6 individene om svak tetthet i brystet eller ubehag klinisk knyttet til luftveisreaktivitet.
Fingolimod kan indusere bradykardi i starten av behandlingen.Pulsen reduseres vanligvis innen en time etter den første dosen og er maksimal innen de første 6 timene. Den negative kronotrope effekten av Gilenya vedvarer utover 6 timer og avtar gradvis i løpet av de følgende behandlingsdagene (se pkt. 4.4 for ytterligere detaljer). Det har vært rapporter om atrioventrikulær ledning som reduseres, med isolerte rapporter om atrioventrikulær blokk. Fullstendig, forbigående og spontan oppløsning (se pkt. 4.4 og 4.8).
Hvis overdosen sammenfaller med den første eksponeringen for Gilenya, er det viktig å ha pasienten kontinuerlig (sanntid) elektrokardiografisk overvåking med timepuls og blodtrykksmålinger, i hvert fall i løpet av de første 6 timene (se pkt. 4.4).
Ytterligere overvåking er også nødvendig (minst til neste morgen og uansett til symptomene er løst) hvis pulsen etter 6 timer etter administrering av den første dosen er
Fingolimod elimineres ikke ved verken dialyse eller plasmaferese.
05.0 FARMAKOLOGISKE EGENSKAPER
05.1 Farmakodynamiske egenskaper
Farmakoterapeutisk gruppe: selektive immunsuppressive midler.
ATC -kode: L04AA27.
Virkningsmekanismen
Fingolimod er en sfingosin-1-fosfat (S1P) reseptormodulator. Ved hjelp av sfingosinkinasen omdannes fingolimod til den aktive metabolitten fingolimodfosfat som ved lave nanomolære konsentrasjoner binder seg til S1P1-reseptoren på lymfocyttoverflaten, og krysser lett blod-hjernebarrieren for å binde seg til reseptoren i sentralnervesystemet system S1P1 plassert på cellene i sentralnervesystemet. Fingolimodfosfat, som fungerer som en funksjonell antagonist av S1P -reseptorer uttrykt på lymfocytter, hemmer lymfocyters evne til å rømme fra lymfeknuter, noe som resulterer i omfordeling i stedet for ødeleggelse av lymfocyttene. Denne omfordelingen reduserer infiltrasjonen av patogene lymfocytter til sentralnervesystemet, der de er involvert i nervebetennelse og vevsskade. Dyreforsøk og eksperimenter in vitro indikerer at fingolimod også kan virke ved å samhandle med S1P -reseptorer uttrykt på celler i sentralnervesystemet.
Farmakodynamiske effekter
I løpet av 4-6 timer etter den første administreringen av fingolimod 0,5 mg, reduseres antallet lymfocytter i det perifere blodet til omtrent 75% av grunnverdien. Ved å fortsette med daglig administrering, fortsetter antallet lymfocytter å synke i to uker og nå en minimumsverdi på omtrent 500 celler / mikroliter, eller omtrent 30% av utgangsverdien. 18% av pasientene nådde en minimumsverdi under 200 celler / mikroliter minst én gang. Ved kontinuerlig daglig behandling forblir antallet lymfocytter lavt. De fleste T- og B -lymfocytter vandrer jevnlig gjennom lymfoide organer: fingolimod virker hovedsakelig på disse cellene. Omtrent 15-20% av T-lymfocytter har en TEM (minneeffektor) fenotype: disse cellene er viktige for perifer immunovervåking. Siden denne typen lymfocytter vanligvis ikke migrerer til lymfoide organer, virker ikke fingolimod på disse cellene. Økningen i antall perifere lymfocytter er tydelig i dagene etter avsluttet behandling med fingolimod; lymfocyttallene går vanligvis tilbake til det normale innen en til to måneder. Kronisk administrering av fingolimod resulterer i en liten nedgang i antall nøytrofiler som tilsvarer omtrent 80% av utgangsverdien Fingolimod virker ikke på monocytter.
Fingolimod forårsaker en forbigående reduksjon i hjertefrekvensen og redusert atrioventrikulær ledning ved oppstart av behandlingen (se pkt. 4.4. Og 4.8). Maksimal reduksjon i hjertefrekvens observeres innen 6 timer etter administrering, med 70% av den negative kronotrope effekten. Med påfølgende administrasjoner går pulsen tilbake til baseline innen en måned. Reduksjonen i hjertefrekvensen indusert av fingolimod kan reverseres ved parenteral administrering av atropin eller isoprenalin. Inhalert salmeterol har også vist seg å ha en beskjeden positiv kronotrop effekt. Når behandling med fingolimod starter, er det en økning i for tidlige atriekontraksjoner, men det er ingen økt frekvens av atrieflimmer / flagre eller ventrikulære arytmier eller ektopi. Behandling med fingolimod resulterer ikke i redusert hjerteeffekt, og påvirker ikke sympatomimetiske responser i hjertet, inkludert variasjon i daglig puls og respons på anstrengelse.
Behandling med fingolimod, enkelt eller gjentatte doser på 0,5 mg og 1,25 mg i to uker, resulterer ikke i en merkbar økning i luftveismotstanden målt som FEV1 og Forced Expiratory Flow (FEF) 25-75. Men med enkeltdoser fingolimod ≥5 mg (10 ganger anbefalt dose) oppstår en doseavhengig økning i luftveismotstand. Behandling med gjentatte doser fingolimod på 0,5 mg, 1,25 mg eller 5 mg fører ikke til svekket oksygenering eller oksygendesaturering under trening eller en økning i luftveisrespons på metakolin. Personer som får fingolimod reagerer med normal bronkodilatasjon til inhalerte beta-agonister.
Klinisk effekt og sikkerhet
Effekten av Gilenya ble demonstrert i to studier som evaluerte en gang daglig administrering av fingolimod 0,5 mg og 1,25 mg hos pasienter med recidiverende remitterende multippel sklerose (RRMS). Begge studiene var påmeldte pasienter som hadde hatt ≥ 2 tilbakefall i de foregående 2 årene eller ≥1 tilbakefall året før. Poengsummen på skalaen for utvidet funksjonshemming (EDSS) var 0-5,5. En tredje studie utført i den samme pasientpopulasjonen ble fullført etter registrering av Gilenya.
I den 2-årige, randomiserte dobbeltblinde kontrollerte placebokontrollerte studien D2301 (FREEDOMS) ble 1272 pasienter inkludert (n = 425 behandlet med fingolimod 0,5 mg, 429 med fingolimod 1,25 mg, 418 med placebo). Medianverdier av baseline -egenskaper var: alder 37 år, sykdomsvarighet 6,7 år, EDSS -score på 2,0. Resultatene er presentert i tabell 1. Det var ingen signifikante forskjeller mellom dosene 0,5 mg og 1,25 mg for alle endepunkter.
Tabell 1: Studie D2301 (FREEDOMS): Hovedresultater
† Progressjon av funksjonshemming definert som 1-punkts økning i EDSS bekreftet etter 3 måneder
** s
Alle kliniske endepunkter ble evaluert ved analyse hensikt å behandle. Analyser relatert til MR -data brukte evaluerbare datasett.
Pasienter som hadde fullført fasen kjerne av 24-måneders FREEDOMS-studien var i stand til å gå inn i den doseblinde forlengelsesfasen (D2301E1) og motta fingolimod. Totalt 920 pasienter kom inn (n = 331 fortsatte med 0,5 mg dosen, 289 ved dosen 1,25 mg, 155 byttet fra placebo til 0,5 mg og 145 fra placebo til 1,25 mg). Etter 12 måneder (måned 36) var 856 pasienter (93%) fortsatt registrert. Mellom måned 24 og måned 36 er den årlige tilbakefallshastigheten (ARR) for pasienter som får fingolimod 0,5 mg i fase kjerne av studien og som hadde fortsatt med samme dose (0,5 mg) var 0,17 (0,21 i fase kjerne av studiet). Den årlige tilbakefallshastigheten for pasienter som byttet fra placebo til fingolimod 0,5 mg var 0,22 (0,42 i fase kjerne av studiet).
Lignende resultater ble oppnådd i en fase III, 2-årig, randomisert, dobbeltblind, placebokontrollert studie (D2309; FREEDOMS 2) utført på 1083 pasienter med tilbakefall-remitterende multippel sklerose (n = 358 behandlet med fingolimod 0, 5 mg , 370 med fingolimod 1,25 mg, 355 med placebo). Medianverdier av baseline -egenskaper var: alder 41 år, sykdomsvarighet 8,9 år, EDSS -score på 2,5.
Tabell 2: Studie D2309 (FREEDOMS 2): Hovedresultater
† Progressjon av funksjonshemming definert som 1-punkts økning i EDSS bekreftet etter 3 måneder
** s
Alle kliniske endepunkter ble evaluert ved analyse hensikt å behandle. Analyser relatert til MR -data brukte evaluerbare datasett.
I studie D2302 (TRANSFORMS), fase III, som varer 1 år, randomisert, dobbeltblind kontrollert og dobbel dummy versus aktivt stoff (interferon beta-1α) 1280 pasienter ble inkludert (n = 429 behandlet med fingolimod 0,5 mg, 420 med fingolimod 1,25 mg, 431 med intramuskulær injeksjon av interferon beta-1α i en dose på 30 mikrogram en gang i uken). Medianverdier av baseline -egenskaper var: alder 36 år, sykdomsvarighet 5,9 år, EDSS -score på 2,0. Resultatene av studien er presentert i tabell 3. Det var ingen signifikant forskjell mellom dosene på 0,5 mg og 1,25 mg med hensyn til studiens endepunkter.
Tabell 3: Studie D2302 (TRANSFORMS): Hovedresultater
† Progressjon av funksjonshemming definert som 1-punkts økning i EDSS bekreftet etter 3 måneder
** s
Alle kliniske endepunkter ble evaluert ved analyse hensikt å behandle. Analyser relatert til MR -data brukte evaluerbare datasett.
Pasienter som hadde fullført fasen kjerne av 12-måneders TRANSFORMS-studien var i stand til å gå inn i den doseblinde forlengelsesfasen (D2302E1) og motta fingolimod. Totalt 1.030 pasienter kom inn, men 3 av disse fikk ikke behandling (n = 356 fortsatte med 0,5 mg dosen, 330 ved dosen 1,25 mg, 167 byttet fra interferon beta-1α til 0, 5 mg og 174 fra interferon beta -1α ved 1,25 mg). Etter 12 måneder (måned 24) var 882 pasienter (86%) fortsatt registrert. Mellom månedene 12 og 24 var den årlige tilbakefallshastigheten (ARR) for pasienter som fikk fingolimod 0,5 mg i fase kjerne av studien og som hadde fortsatt med samme dose (0,5 mg) var 0,20 (0,19 i fase kjerne av studiet). Den årlige tilbakefallshastigheten for pasienter som byttet fra interferon beta-1α til fingolimod 0,5 mg var 0,33 (0,48 i fase kjerne av studiet).
Sammenslåtte resultater fra studier D2301 og D2302 viste en konsekvent og statistisk signifikant reduksjon fra kontroll av den årlige tilbakefallsfrekvensen i undergrupper definert av kjønn, alder, tidligere MS -terapi, sykdomsaktivitet eller funksjonshemming ved baseline.
Ytterligere analyse av resultater fra kliniske studier viser signifikante behandlingseffekter i undergrupper av pasienter med svært aktiv tilbakefall-remitterende multippel sklerose.
Det europeiske legemiddelkontoret (European Medicines Agency) har utsatt forpliktelsen til å levere resultatene av studier med Gilenya i en eller flere undergrupper av den pediatriske populasjonen i multippel sklerose (se pkt. 4.2 for informasjon om pediatrisk bruk).
05.2 "Farmakokinetiske egenskaper
Farmakokinetiske data ble innhentet hos friske frivillige, pasienter med nyretransplantasjon og pasienter med multippel sklerose.
Den farmakologisk aktive metabolitten som er ansvarlig for effekten er fingolimodfosfat.
Absorpsjon
Absorpsjon av fingolimod skjer sakte (Tmax på 12-16 timer) og er omfattende (≥85%). Den tilsynelatende absolutte biotilgjengeligheten etter oral administrering er 93%(konfidensintervall: 79-111%). Konsentrasjoner blod ved stabil nivåer oppnås innen 1-2 måneder etter administrering av daglige enkeltdoser av fingolimod og legeringsnivåer stabil de er omtrent 10 ganger høyere enn de som ble sett med startdosen.
Matinntak endrer ikke toppkonsentrasjonen (Cmax) eller systemisk eksponering (AUC) for fingolimod. Fingolimod fosfat Cmax ble litt økt med 34% mens AUC var uendret. Derfor kan Gilenya tas enten på full eller tom mage (se pkt. 4.2).
Fordeling
Fingolimod fordeler seg raskt i røde blodlegemer, og er tilstede i 86% av blodcellene. Fingolimodfosfat har en 17% lavere fordeling av røde blodlegemer. Plasmaproteinbinding av fingolimod og fingolimodfosfat er høy (> 99%).
Fingolimod er omfattende distribuert i vev med et distribusjonsvolum på omtrent 1200 ± 260 liter.
Biotransformasjon
Hos mennesker metaboliseres fingolimod ved reversibel stereoselektiv fosforylering med dannelse av den farmakologisk aktive (S) -enantiomeren av fingolimodfosfat. Fingolimod elimineres ved oksidativ biotransformasjon, hovedsakelig katalysert av CYP4F2 og muligens andre isoenzymer, og påfølgende nedbrytning til inaktive metabolitter, tilsvarende fettsyrer. Det ble også observert dannelse av farmakologisk inaktive ikke-polare ceramid-analoger av fingolimod. Det viktigste enzymet som er involvert i metabolismen av fingolimod er delvis identifisert og kan være CYP4F2 eller CYP3A4.
Etter en enkelt oral administrering av fingolimod [14C], er hovedkomponentene knyttet til fingolimod, oppdaget i blodet ved deres bidrag til AUC opptil 34 dager etter administrering av de totale radiomerkede komponentene, selve fingolimod (23%), fingolimodfosfat ( 10%) og noen inaktive metabolitter (M3 karboksylsyremetabolitt (8%), M29 ceramidmetabolitt (9%) og M30 ceramidmetabolitt (7%)).
Eliminering
Blodklaring av fingolimod er 6,3 ± 2,3 L / t og gjennomsnittlig eliminasjonshalveringstid (t1 / 2) er 6-9 dager. Blodnivået av fingolimod og fingolimodfosfat reduseres parallelt i terminalfasen, og resulterer dermed i lignende halvpart -lever for begge molekylene.
Etter oral administrering utskilles omtrent 81 % av dosen sakte i urinen som inaktive metabolitter Fingolimod og fingolimodfosfat skilles ikke ut uendret i urinen, men er tilstede som hovedkomponenter i avføringen, hvor mengder hver representerer mindre enn 2,5 % av dosen . Etter 34 dager er utvinningen av den administrerte dosen 89%.
Linjæritet
Konsentrasjonene av fingolimod og fingolimodfosfat øker tilsynelatende doseproporsjonalt etter gjentatt administrering av enkeltdoser på 0,5 mg eller 1,25 mg.
Kjennetegn i spesifikke populasjoner
Farmakokinetikken til fingolimod og fingolimodfosfat er ikke differensiert mellom menn og kvinner, hos pasienter med forskjellig etnisk opprinnelse eller hos pasienter med lett til alvorlig nedsatt nyrefunksjon.
Hos personer med mild, moderat eller alvorlig nedsatt leverfunksjon (Child-Pugh klasse A, B og C) ble det ikke observert endring i fingolimod Cmax, mens fingolimod AUC økte med 12%, 44%og 103%. Hos pasienter med alvorlig nedsatt leverfunksjon ( Child-Pugh klasse C), fingolimodfosfat Cmax ble redusert med 22% og AUC ble ikke vesentlig endret. Farmakokinetikken til fingolimodfosfat er ikke evaluert hos pasienter med mild til moderat nedsatt leverfunksjon. Den tilsynelatende eliminasjonshalveringstiden for fingolimod var uendret hos personer med lett nedsatt leverfunksjon, mens den ble økt med omtrent 50% hos pasienter med moderat eller alvorlig nedsatt leverfunksjon.
Fingolimod må ikke brukes til pasienter med alvorlig nedsatt leverfunksjon (Child-Pugh klasse C) (se pkt. 4.3). Fingolimodbehandling bør startes med forsiktighet hos pasienter med mild til moderat nedsatt leverfunksjon (se pkt.4.2).
Klinisk erfaring og farmakokinetiske data fra pasienter over 65 år er begrenset.Gilenya bør brukes med forsiktighet hos pasienter over 65 år (se pkt. 4.2).
Pediatrisk populasjon
Data fra en nyretransplantasjonsstudie inkludert 7 barn over 11 år er begrenset (studie FTY720A0115). Sammenligning av disse dataene med friske voksne frivillige har liten relevans, og det kan ikke trekkes noen meningsfulle konklusjoner om de farmakokinetiske egenskapene til fingolimod hos barn.
05.3 Prekliniske sikkerhetsdata
Den prekliniske sikkerhetsprofilen til fingolimod ble evaluert hos mus, rotter, hunder og aper. Hovedmålorganene var lymfoidsystemet (lymfopeni og lymfoide atrofi), lungene (vektøkning, glatt muskelhypertrofi ved bronkioloalveolært kryss), og i forskjellige arter hjertet (negativ kronotrop effekt, økt blodtrykksblod, perivaskulære endringer og myokardialt) degenerasjon); i en 2-årig studie var fingolimod aktiv på blodkar (vaskulopati) bare hos rotter ved doser på 0,15 mg / kg og over, tilsvarende omtrent 4 ganger den menneskelige systemiske eksponeringen (AUC) ved en daglig dose på 0,, 5 mg.
Det ble ikke observert tegn på karsinogenitet i en 2-årig studie på rotter med orale doser fingolimod opp til maksimal tolerert dose på 2,5 mg / kg, noe som representerer en margin på omtrent 50 ganger den humane systemiske eksponeringen (AUC) ved en dose på 0,5 mg. Imidlertid ble det i en 2-årig studie på mus observert en høyere forekomst av malignt lymfom ved doser på 0,25 mg / kg og høyere, tilsvarende omtrent 6 ganger den menneskelige eksponeringen. Systemisk (AUC) ved en daglig dose på 0,5 mg.
I dyreforsøk ble det ikke funnet at fingolimod var mutagent eller klastogent.
Fingolimod hadde ingen effekt på sædceller / motilitet eller fruktbarhet hos hann- og hunnrotter opp til maksimal testet dose (10 mg / kg), noe som representerer en margin på omtrent 150 ganger den humane systemiske eksponeringen (AUC) ved en daglig dose på 0,5 mg.
Fingolimod ble vist å være teratogent hos rotter ved administrering i doser på 0,1 mg / kg eller høyere. De vanligste føtale viscerale misdannelsene inkluderer vedvarende arteriell stamme og ventrikelseptumdefekt. Det teratogene potensialet hos kaniner kan ikke vurderes fullt ut, men økt embryo-fosterdødelighet ble observert ved doser på 1,5 mg / kg og over, og reduserte levedyktige fostre samt fostervekstretardasjon ved doser på 5 mg / kg. Kg.
Hos rotter ble overlevelsen til F1 -generasjonen av unger redusert tidlig i fødselsperioden ved doser som ikke forårsaket mors toksisitet. F1 -generasjonen var imidlertid upåvirket av fingolimod -behandling med hensyn til kroppsvekt, utvikling, oppførsel og fruktbarhet.
Fingolimod ble utskilt i melken til behandlede lakterende dyr Fingolimod og dets metabolitter krysset placentabarrieren hos drektige kaniner.
Vurdering av miljørisiko (Vurdering av miljørisiko, VAR)
Det forventes ingen miljørisiko ved bruk av Gilenya hos pasienter med tilbakefallende multippel sklerose.
06.0 LEGEMIDDELOPPLYSNINGER
06.1 Hjelpestoffer
Kapselinnhold:
Magnesiumstearat
Mannitol
Kapselskall:
Gult jernoksid (E172)
Titandioksid (E171)
Gelé
Blekk:
Lakk (E904)
Dehydrert alkohol
Isopropylalkohol
Butylalkohol
Propylenglykol
Renset vann
Konsentrert ammoniakkløsning
Kaliumhydroksyd
Svart jernoksid (E172)
Gult jernoksid (E172)
Titandioksid (E171)
Dimetikon
06.2 Uforlikelighet
Ikke relevant.
06.3 Gyldighetsperiode
2 år.
06.4 Spesielle forholdsregler for lagring
Må ikke oppbevares over 25 ° C.
Oppbevares i originalpakningen for å beskytte medisinen mot fuktighet.
06.5 Emballasje og innhold i pakningen
Pakninger som inneholder 7, 28 eller 98 harde kapsler eller flerpakninger som inneholder 84 (3 pakninger med 28) i blister av PVC / PVDC / aluminium.
Pakninger som inneholder 7 x 1 harde kapsler i perforerte enhetsdoseblister i PVC / PVDC / aluminium.
Det er ikke sikkert at alle pakningsstørrelser blir markedsført.
06.6 Bruksanvisning og håndtering
Ingen spesielle instruksjoner.
07.0 INNEHAVER AV MARKEDSFØRINGSTILLATELSE
Novartis Europharm Limited
Wimblehurst Road
Horsham
West Sussex, RH12 5AB
Storbritannia
08.0 NUMMER FOR MARKEDSFØRINGSTILLATELSE
EU / 1/11/677 / 001-006
040949012
040949024
040949036
040949048
040949051
09.0 DATO FOR FØRSTE GODKJENNELSE ELLER FORNYELSE AV GODKJENNINGEN
17.03.2011
10.0 DATO FOR REVISJON AV TEKSTEN
Juni 2014