Hva er Foscan?
Foscan er en injeksjonsvæske, oppløsning som inneholder virkestoffet temoporfin (1 eller 4 mg / ml).
Hva brukes Foscan til?
Foscan brukes til å lindre symptomene på plateepitelkarsinom i avansert stadium i hode og nakke (en type kreft som starter i cellene som strekker munnen, nesen, halsen eller øret). Det brukes hos pasienter med andre behandlinger er ingen lenger effektive og er ikke egnet for strålebehandling (strålebehandling), kirurgi eller systemisk kjemoterapi (legemidler som brukes ved behandling av kreft; "systemisk" betyr at de er ment å virke på hele kroppen).
Medisinen kan bare fås på resept.
Hvordan brukes Foscan?
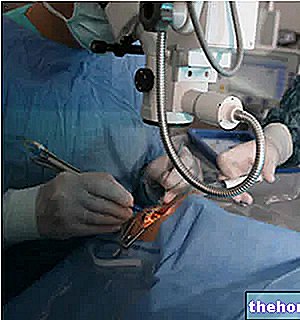
Foscan skal bare administreres på et senter spesialisert på kreftbehandling, der et team kan evaluere pasientens behandling under tilsyn av en lege med erfaring fra fotodynamisk terapi (behandling som bruker lysets virkning). Behandling med Foscan er en to-trinns prosess: stoffet administreres først og aktiveres deretter med en laser. Legemidlet gis gjennom en permanent intravenøs kanyle (et tynt rør satt permanent inn i en vene) i en enkelt sakte injeksjon over en periode på ikke mindre enn seks minutter. Dosen er 0,15 mg per kilo kroppsvekt. Fire dager senere skal hele området som er påvirket av svulsten belyses, opptil 0,5 cm utover den omkringliggende marginen, med et lys generert av en laserkilde ved en bestemt bølgelengde i omtrent 3 minutter og 20 sekunder. Ved hjelp av en fiberoptisk kabel. Hvert område av tumorvev bør kun belyses én gang under hver behandling. Under behandlingen bør de andre områdene av kroppen beskyttes mot lys, slik at stoffet bare aktiveres på svulsten. Hvis en annen syklus er nødvendig, bør den gjøres med et minimumsintervall på fire uker.
Hvordan fungerer Foscan?
Den aktive ingrediensen i Foscan, temoporfin, er et fotosensibiliserende middel (stoff som endres når det utsettes for lys). Etter injeksjon av Foscan distribueres temoporfin gjennom hele kroppen, inkludert svulstmassen. Når det er opplyst med laserlyset på ett
gitt bølgelengde, blir temoporfin aktivert og reagerer med oksygenet som er tilstede i cellene, og skaper en svært reaktiv og giftig type oksygen. Det dreper celler ved å reagere med komponentene (proteiner og DNA) og ødelegge dem. Ved å begrense belysningen til svulsten, er bare tumorcellene skadet, uten å påvirke andre deler av kroppen.
Hvordan har Foscan blitt studert?
Foscan har blitt studert i fire hovedstudier med totalt 409 pasienter med hode- eller nakkekreft. De tre første studiene hadde som mål å undersøke om kreften ble fjernet etter opptil tre behandlingsforløp med Foscan hos totalt 189 pasienter. Den fjerde studien fokuserte på symptomreduksjon hos 220 pasienter med avansert hode- og nakkekreft som ikke kunne opereres eller strålebehandling. I alle studiene ble respons på behandling vurdert mellom 12. og 16. uke etter den siste syklusen med Foscan; Foscan ble imidlertid ikke sammenlignet med andre legemidler.
Hvilken fordel har Foscan vist under studiene?
Resultatene av de tre første studiene virket ikke tilstrekkelige til å bekrefte effekten av Foscan ved utryddelse av kreft i hode og nakke.På den annen side viste 28 pasienter (22%) av de 128 observerte individene en signifikant forbedring av de mest plagsomme symptomene i studien som evaluerte forbedringen av symptomer hos pasienter med kreft i hode og nakke i et langt stadium. En reduksjon i tumorstørrelse ble også observert hos omtrent en fjerdedel av pasientene som var involvert i denne studien.
Hva er risikoen forbundet med Foscan?
De vanligste bivirkningene med Foscan (sett hos mer enn 1 av 10 pasienter) er smerter på injeksjonsstedet, i svulsten eller i ansiktet, blødning, arrdannelse, nekrose i munnen (celledød eller vev i munnen) , dysfagi (svelgeproblemer), ødem i ansiktet (hevelse) og forstoppelse For fullstendig liste over bivirkninger rapportert med Foscan, se pakningsvedlegget.
Foscan må ikke brukes til personer som kan være overfølsomme (allergiske) mot temoporfin eller noen av ingrediensene. Foscan må ikke brukes til pasienter med porfyri (manglende evne til å metabolisere porfyriner), andre sykdommer som forverres av lys, porfyrinallergi eller svulster som sprer seg til et blodkar eller er nær belysningsstedet. Foscan må heller ikke gis til pasienter som skal opereres i løpet av de neste 30 dagene, til pasienter med øyesykdom som krever en "spaltelampe" -evaluering (et verktøy som brukes av øyeleger for å se i øyet). "Øye) for de neste 30 dagene eller til pasienter som allerede er i behandling med et annet legemiddel som øker lysfølsomheten.
I seks måneder etter injeksjonen av Foscan bør pasientene unngå eksponering for sterkt lys for å unngå risiko for hudforbrenning. For mer informasjon, se pakningsvedlegget.
Hvorfor har Foscan blitt godkjent?
Komiteen for medisiner for mennesker (CHMP) konkluderte med at effekten av Foscan for å lindre symptomer forbundet med avansert hode- og nakkekreft var bemerkelsesverdig. Derfor bestemte komiteen at fordelene med Foscan er større enn risikoen for palliativ behandling av pasienter med avansert plateepitelkarsinom i hode og nakke som har sviktet tidligere behandlinger og ikke er egnet for strålebehandling, kirurgi eller systemisk cellegift. Komiteen anbefalte frigjøring av markedsføringstillatelsen for Foscan.
Foscan ble opprinnelig autorisert under "eksepsjonelle omstendigheter" fordi, på grunn av det faktum at sykdommen er sjelden og av vitenskapelige årsaker, informasjon var knapp på tidspunktet for autorisasjonen. Siden selskapet ga tilleggsinformasjonen som ble bedt om, var begrensningen på de "eksepsjonelle omstendighetene" "ble fjernet 21. mai 2008.
Mer informasjon om Foscan:
24. oktober 2001 utstedte EU -kommisjonen en "markedsføringstillatelse" for Foscan, gyldig i hele EU. "Markedsføringstillatelsen" for
handelen ble fornyet 24. oktober 2006. Innehaver av markedsføringstillatelsen er selskapet Biolitec Pharma ltd.
For hele versjonen av Foscan EPAR klikk her.
Siste oppdatering av dette sammendraget: 05-2008
Informasjonen om Foscan - temoporfin som er publisert på denne siden kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.