MERK: MEDISINSK PRODUKT IKKE LENGRE GODKJENT
Hva er TESLASCAN?
TESLASCAN er en løsning for intravenøs infusjon (drypp i en vene) som inneholder virkestoffet mangafodipir trinatrium.
Hva brukes TESLASCAN til?
TESLASCAN er kun beregnet på diagnostisk bruk. TESLASCAN brukes til pasienter som gjennomgår magnetisk resonansavbildning (MR) for å påvise leverskader som kan være forårsaket av leverkreft eller metastaser (migrasjon av kreftceller fra et hovedfokus). TESLASCAN er et "kontrastmedium" som brukes for å få skarpere bilder. TESLASCAN kan også brukes i forbindelse med MR for å hjelpe til med undersøkelse av bukspyttkjerteleskader.
Medisinen kan bare fås på resept.
Hvordan brukes TESLASCAN?
TESLASCAN skal brukes ved intravenøs administrering i en dose på 0,5 ml per kilo kroppsvekt. Infusjonshastigheten er 2-3 ml / min for leverdiagnostisk test og 4-6 ml / min for bukspyttkjerteldiagnostisk test. Kontrastforsterkning observeres 15-20 minutter etter "infusjonens start og beholdes i omtrent 4 timer. For mer informasjon, se pakningsvedlegget.
Hvordan fungerer TESLASCAN?
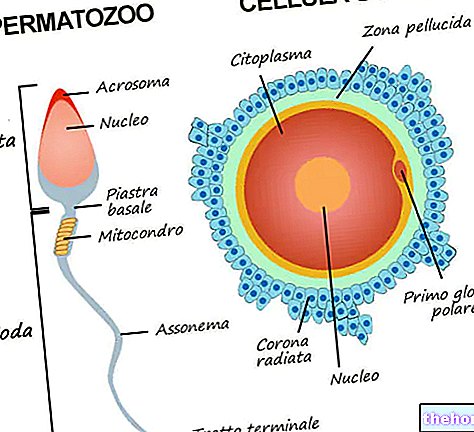
Virkestoffet i TESLASCAN, mangafodipir, inneholder mangan, et kjemisk element fra gruppen av metaller. Mangan brukes som kontrastmiddel for å få bedre bilder med magnetiske resonansdiagnostiske enheter. MR er en diagnostisk avbildningsteknikk som bruker magnetiske felt og radiobølger. Vannmolekylene i kroppen er følsomme for magnetfelt og produserer et bestemt signal når radiobølger sendes ut. Mangan interagerer med vannmolekylene. Som et resultat av denne interaksjonen overfører vannmolekylene et sterkere signal, noe som resulterer i et skarpere bilde.
I TESLASCAN er mangan bundet til "et annet kjemikalie for å danne et" chelat. "Etter at medisinen er injisert, frigjøres mangan i blodet og absorberes av normale lever- og bukspyttkjertelvev mer effektivt enn kreftceller. På denne måten er det mulig å oppdage forskjellen mellom normalt og sykt vev.
Hvordan har TESLASCAN blitt studert?
Studier av TESLASCAN ved MR for leverskader ble utført hos 617 pasienter. Pasientene hadde en til fem leverskader som allerede var identifisert med MR, ultralyd eller computertomografi (CT). Disse pasientene ble utført med en MR -skanning optimalisert med TESLASCAN. mål på effektivitet var forskjellen i antall leverskader påvist ved bruk av TESLASCAN med MR sammenlignet med forrige skanning.
Studier for bukspyttkjertelsykdom ble utført hos 292 pasienter og sammenlignet effektiviteten av TESLASCAN-optimalisert MR versus spiral CT, en annen diagnostisk metode som ble brukt for å påvise bukspyttkjerteleskader. Hovedmål for effektivitet var basert på samsvar mellom diagnosen som ble stilt på grunnlag av skanningene og de faktiske lesjonene som ble funnet under operasjon eller biopsi.
Hvilken fordel har TESLASCAN vist under studiene?
Når det gjelder leverskader, tillot bruk av MR med TESLASCAN påvisning av flere lesjoner. Totalt sett ble det påvist flere lesjoner hos 33% av pasientene under studiene, men hos 20% av pasientene var det færre lesjoner. bukspyttkjertelen, optimalisert MR med TESLASCAN viste seg å være mer effektiv enn spiral CT.
Hva er risikoen forbundet med TESLASCAN?
De hyppigst rapporterte bivirkningene med TELESCAN (sett hos mellom 1 og 10 av 100 pasienter) er hodepine, kvalme, rødme og varmefølelse. For fullstendig liste over bivirkninger rapportert for TESLASCAN, se pakningsvedlegget.
TESLASCAN må ikke brukes til personer som kan være overfølsomme (allergiske) overfor mangafodipir trinatrium eller noen av de andre stoffene. TESLASCAN må ikke brukes til gravide eller ammende, til pasienter med feokromocytom (en svulst i binyrene) eller til pasienter med alvorlige lever- eller nyreproblemer.
Hvorfor har TESLASCAN blitt godkjent?
Komiteen for medisiner for mennesker (CHMP) bestemte at fordelene med TESLASCAN er større enn risikoen ved bruk som kontrastmiddel for magnetisk resonansavbildning (MR), for påvisning av leverskade antagelig på grunn av sykdom metastatisk eller hepatocellulært karsinom, som samt i tillegg til MR for å hjelpe til med å undersøke fokale lesjoner i bukspyttkjertelen. Utvalget anbefalte derfor å gi markedsføringstillatelse for produktet.
Mer informasjon om TESLASCAN
22. mai 1997 ga EU -kommisjonen GE Healthcare AS en "markedsføringstillatelse" for TESLASCAN, gyldig i hele EU. "Markedsføringstillatelsen" ble fornyet 22. mai 2002 og 22. mai 2007.
For hele versjonen av TESLASCAN EPAR klikk her.
Siste oppdatering av denne oppsummeringen: 04-2007.
Informasjonen om TESLASCAN - mangafodipir trisodio publisert på denne siden kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.