Generellitet
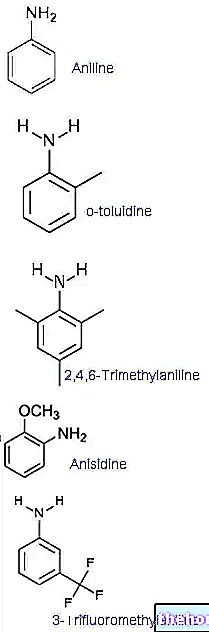
Cyanid er det kjemiske uttrykket som identifiserer enhver kjemisk forbindelse som inneholder cyanogruppen (CN).
Cyangruppen er et molekyl dannet ved forening av et karbonatom og et nitrogenatom.

Eksempler på uorganisk cyanid er hydrogencyanid, natriumcyanid, kaliumcyanid og cyanogenklorid.
Eksempler på organisk cyanid, derimot, er nitriler, som finnes i kjernene til forskjellige frukter (aprikoser, fersken, kirsebær, etc.).
Cyanider er kjemikalier som er mye brukt i produksjon, fra papirindustrien til metallurgi, plast, etc.
Hva er cyanid?
Et cyanid er en hvilken som helst kjemisk forbindelse som inneholder cyanogruppen (CN).
Cyanogruppen er resultatet av foreningen av et karbonatom (C i CN) til et nitrogenatom (N i CN). Bindingen som forener karbon til nitrogen er en trippel kovalent binding. Den totale ladningen som er tilstede på CN -gruppen er negativ, derfor er cyanogruppen et anion.
CYANIDE SOM GIFT: UORGANISK CYANID
I den vanlige fantasien refererer begrepet cyanid til en kraftig gift med dødelige effekter.
Kjemisk sett er cyanidene som virker som potente giftstoffer uorganiske cyanider, for eksempel natriumcyanid (NaCN), kaliumcyanid (KCN) og cyanogenklorid (ClCN).
HVOR KOMMER UORGANISK CYANID FRA?
Enhver type uorganisk cyanid stammer fra dissosiasjonen av hydrogensyanid (HCN eller hydrogensyanid) eller et av dets salt (som igjen kan være et cyanid).
Hydrogencyanid er et uorganisk molekyl, resultatet av foreningen av en cyanogruppe (CN) med et hydrogenatom (H). Det er en svært giftig svak syre og kan betraktes som et spesielt eksempel på uorganisk cyanid.
Vær oppmerksom på: natriumcyanid og kaliumcyanid er to salter av hydrogencyanid.
Cyanogenklorid, derimot, er et derivat av et salt av hydrogencyanid; for å være presis er det et derivat av natriumcyanid. Oksidasjonen av natriumcyanid med klor danner cyanogenklorid.
ORGANISK CYANIDE
I naturen danner cyanoanionen CN også kjemiske forbindelser med organiske molekyler (f.eks. Metylgrupper, etc.), noe som gir opphav til typer organisk cyanid.
Også kjent som nitriler, organiske cyanider er lett giftige eller blir bare giftige ved visse anledninger; de er imidlertid mindre og mindre giftige enn uorganiske cyanider.

Eiendom
Egenskapene til et cyanid avhenger av hvilke atomer som er bundet til CN -cyanogruppen.
Hydrocyansyre er en lyseblå eller fargeløs væske ved romtemperatur, mens den er en fargeløs gass ved høye temperaturer. Både i flytende og gassform har den en lukt som ligner den av bitre mandler.
Natriumcyanid og kaliumcyanid fremstår som hvitt pulver og avgir - som hydrogencyanid - en lukt som kan sammenlignes med den av bitre mandler.
Cyanogenklorid er en fargeløs flytende gass, tyngre enn luft og med en bestemt skarp lukt.
Hvor er det?
I naturen, så vel som i kjernene til noen frukter, er cyanid også til stede i forskjellige plantearter; planter holder den i bladene og / eller i barken og bruker den til å forsvare seg mot planteetere.
I tillegg til planter er andre levende ting som produserer cyanid (eller stoffer som inneholder CN -cyanogruppen) noen bakterier og noen sopp.
CYANIDE SOM ET FORBRENNINGSPRODUKT
Hydrogencyanid er et mulig produkt av forbrenningsprosesser.
For å være presis, er den tilstede i eksosen til forbrenningsmotorer, i sigarettrøyken som dannes under forbrenningen av sistnevnte og i røykene som kommer fra sammensmelting av plastmaterialer basert på akrylonitril (en organisk forbindelse, som inneholder en cyano gruppe CN).
Bruker
I produksjonen er cyanid mye brukt. Faktisk papirindustrien (for å produsere papir), tekstilindustrien (for å produsere tekstiler, etc.), industrien for produksjon av plast, fotografisk industri (for å produsere alle de kjemiske forbindelsene for utvikling av bildene), metallurgisk industri (for å produsere stål og jern, for å vaske metaller og for galvanisering), industrien som behandler behandling av avløpsvann og industrien for produksjon av plantevernmidler (mot parasitter, etc.) for ulike typer miljø.
Av åpenbare årsaker kan det finnes spor av cyanid i avfallsproduktene fra alle de nevnte aktivitetene.
SISTE BRUK
Tidligere fant hydrogencyanid bruk for tragiske formål.
For eksempel, under andre verdenskrig, brukte Nazi -Tyskland det - under navnet Zyklon B - som et giftig middel i gasskamrene i dødsleirene.
Spredning
Cyanid har evnen til å spre seg i vann, jord og luft (N.B: i luften er det i form av gass).
Mennesker kan komme i kontakt med cyanid ved å puste forurenset luft, drikke forurenset vann, spise forurenset mat eller berøre forurenset jord.
En "daglig" cyanidkilde - som mange mennesker utsettes for - er sigarettrøyk.
Effekter
Etter eksponering tar det lite tid for cyanid å komme inn i blodet og spre seg gjennom kroppen via blodet.
Menneskekroppen reagerer på tilstedeværelsen av cyanid på forskjellige måter, avhengig av om dosene er veldig lave eller middels høye.
Når dosene er veldig lavecyanid omdanner gjennom en rekke cellulære reaksjoner til tiocyanat, en kjemisk forbindelse som er ufarlig for helse og som mennesket eliminerer gjennom urinen. Videre, alltid i lave doser, kombineres cyanid med vitamin B12 og det resulterende binomiet ser ut til å har gunstige effekter på både nerveceller og blodceller.
Når derimot doser er middels til høye, evnen til den menneskelige organismen til å omdanne cyanid til tiocyanat blir undertrykt (på grunn av overdreven arbeidsmengde), og det aktuelle giftige stoffet forhindrer cellene i å bruke oksygenet. "Oksygen fører til cellens død.
Hjertet, luftveiene og sentralnervesystemet påvirkes mest av en stor eksponering for cyanid.
Vær oppmerksom på: For å unngå tvil bør det bemerkes at kronisk eksponering for svært små doser cyanid kan ha toksiske effekter som ligner dem som er forårsaket av eksponering for middels høye doser.
Toksisitet
De toksiske effektene av cyanid på menneskers helse avhenger av tre faktorer: dosen av giftig stoff som en har kommet i kontakt med, eksponeringens varighet og typen cyanid.
Eksponering for mellomdoser av cyanid innebærer vanligvis:
- Akselerasjon av pusten;
- Følelse av rastløshet;
- Svimmelhet;
- Følelse av svakhet;
- Hodepine
- Kvalme og følelse av oppkast
- Akselerasjon av hjerteslag.
Hvis cyaniddosene er høye, er de nevnte manifestasjonene forbundet med:
- Kramper;
- Hypotensjon;
- Bremsing av hjerterytmen
- Tap av bevissthet;
- Kortpustethet og pustevansker på grunn av lungeproblemer
- Hjertestans.
Effektene av eksponering for cyanid begynner å vise seg etter bare noen få sekunder / minutter.Dosen påvirker hovedsakelig hastigheten til effektene begynner.
Vanligvis oppstår død av cyanideksponering som følge av alvorlig respirasjonssvikt eller hjertestans.
LANGTIDSEFFEKT
Ifølge flere kliniske undersøkelser vil mennesker som overlever "massiv cyanideksponering, ha en tendens til å utvikle permanente nevrologiske problemer, hvorav noen etterligner symptomer som er veldig like de ved Parkinsons sykdom."
LETHAL DOSE
Når doser cyanid er dødelige, snakker eksperter om "død av cyanidforgiftning".
For natriumcyanid og kaliumcyanid er den dødelige dosen for mennesker 200-300 mg; for hydrogencyanid, derimot, er den dødelige dosen for mennesker 50 mg.
Terapi
Eksponering for giftige doser cyanid representerer en medisinsk nødssituasjon som skal behandles veldig raskt og på den mest hensiktsmessige måten.
Generelt er de aller første terapeutiske indikasjonene:
- Flytt deg så raskt som mulig fra eksponeringsstedet / miljøet og flytt til et uforurenset sted;
- Ta av deg klærne i tilfelle de er forurenset, og legg dem tilbake i en plastpose;
- Vask øynene hvert 10-15 minutt hvis de brenner seg;
- Vask alle deler av huden som har kommet i kontakt med cyanidet med såpe og vann;
- Ring for medisinsk hjelp.
Når medisinsk hjelp kommer, vil de fullføre behandlingen, gi oksygen til den aktuelle personen og en motgift.
Motgiftene mot eksponering for store doser cyanid er natriumtiosulfat, natriumnitritt og hydroksokobalamin.