MERK: LEGEMIDLET ER IKKE LENGRE GODKJENT
Kjennetegn ved medisinen
Preotact består av et hvitt pulver og et løsningsmiddel i en patron, som skal reduseres til en injeksjonsvæske, oppløsning med en spesiell penn. Den aktive ingrediensen i Preotact er parathyroidhormon.
Terapeutiske indikasjoner
Preotact brukes til å behandle osteoporose (en sykdom som gjør bein skjøre) hos postmenopausale kvinner med høy risiko for brudd.Preotact har vist seg å redusere brudd i ryggraden betydelig, men ikke hoftebrudd. Medisinen kan bare fås på resept.
Hvordan å bruke
Den anbefalte dosen er 100 mikrogram Preotact, administrert en gang daglig ved subkutan (under huden) injeksjon i magen. Når patronen settes inn i den spesielle injeksjonspennen og skrus på, blandes pulveret og væsken og danner injeksjonsvæsken. Når de nødvendige instruksjonene for riktig injeksjon er mottatt (brukerhåndbok følger med pennen), kan pasientene injisere løsningen selv. Pasienter kan også trenge å ta kalsiumtilskudd og vitamin D hvis de ikke får nok av disse elementene i dietten Preotact kan brukes i opptil 24 måneder, hvoretter pasienter kan behandles med et bisfosfonat (et legemiddel som reduserer bentap).
Handlingsmekanismer
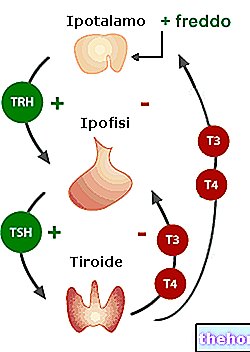
Osteoporose oppstår når det ikke er nok nytt bein til å erstatte det som konsumeres naturlig. Bein blir gradvis tynnere og sprøere og mer utsatt for brudd (brudd). Osteoporose er mer vanlig hos kvinner etter overgangsalderen, når nivåene av det kvinnelige hormonet østrogen stuper. Preotact inneholder parathyroidhormonet, som stimulerer dannelsen av beinvev ved å virke på osteoblaster (cellene som brukes til dannelse av beinvev). Videre øker dette stoffet absorpsjonen av kalsium i maten og forhindrer at overdreven mengde kalsium går tapt i urinen Den aktive ingrediensen i Preotact, parathyroidhormonet, er identisk med det humane parathyroidhormonet og produseres ved en kjent metode som 'rekombinant DNA -teknologi', er dette hormonet laget av en bakterie som har mottatt et gen (DNA) som gjør at det kan produsere det.
Studier utført
I hovedstudien som involverte dette stoffet, som inkluderte 2532 kvinner med postmenopausal osteoporose, ble Preotact sammenlignet med placebo (en dummy -behandling). Frekvensen av vertebrale brudd etter 18 måneders behandling var hovedmål for effektivitet. Omtrent to tredjedeler av kvinnene fortsatte å ta Preotact i opptil 2 år og fikk målt bentettheten. Ben tetthet var hovedmål for effektivitet i en annen studie, som så på bruk av Preotact alene eller i kombinasjon med alendronat (et bisfosfonat).
Fordeler funnet etter studiene
Etter 18 måneder var det 42 vertebrale brudd (3,37%) i placebogruppen og 17 (1,32%) i Preotact -gruppen. Disse dataene viser at, sammenlignet med placebo, reduserer Preotact risikoen for vertebral brudd betydelig hos kvinner som tar det. Risikoreduksjonen var mer markert hos kvinner som tidligere hadde hatt et vertebralbrudd tidligere og hos de som hadde en lav vertebral bentetthet score i starten av studien, noe som indikerer en mer skjør ryggrad. Økninger i bentetthet ble også observert. Studien om kombinert bruk av Preotact og alendronat viste at ved å administrere alendronat etter Preotact er det mulig å øke bentettheten ytterligere.
Tilhørende risiko
De vanligste bivirkningene er hyperkalsemi (økt kalsiumnivå i blodet), hyperkalsinuri (økt kalsiumnivå i urinen) og kvalme. For fullstendig liste over bivirkninger rapportert ved bruk av Preotact, se pakningsvedlegget.
Preotact må ikke brukes til personer som kan være overfølsomme (allergiske) mot parathyroidhormon eller noen av de andre ingrediensene. Det må heller ikke brukes til pasienter som:
• har gjennomgått strålebehandling mot beinene,
• er påvirket av en lidelse som påvirker "balansen mellom kalsium i kroppen",
• har en annen bensykdom enn osteoporose,
• har uforklarlig høye nivåer av alkalisk fosfatase (et enzym),
• har alvorlig nyre- eller leversykdom.
Årsaker til godkjenning
Komiteen for medisiner for mennesker (CHMP) bestemte at fordelene til Preotact er større enn risikoen for behandling av osteoporose hos postmenopausale kvinner med høy risiko for brudd. Derfor anbefalte utvalget at Preotact skulle gis autorisasjon til å inngå
handel.
Mer informasjon
April 2006 ga EU -kommisjonen Nycomed Danmark ApS en "markedsføringstillatelse" for Preotact, gyldig i hele EU.
For hele Preotact -evalueringen (EPAR) -versjonen, klikk her.
Siste oppdatering av dette sammendraget: mars 2006.
Informasjonen om Preotact - parathyroidhormon publisert på denne siden kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.