Hva er Stayveer - Bosentan og hva brukes det til?
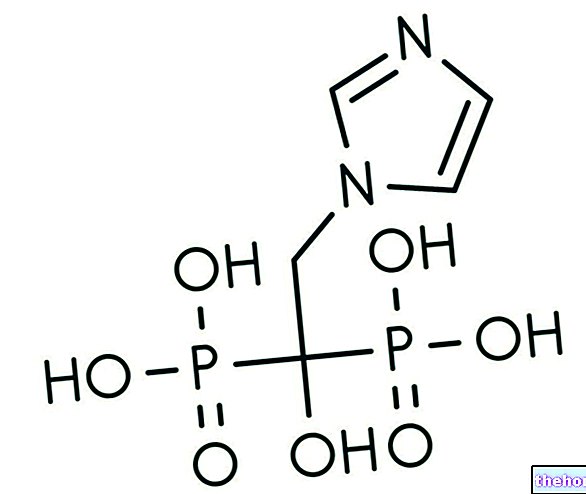
Stayveer er et legemiddel som inneholder virkestoffet bosentan. Det er indisert for behandling av pasienter med klasse III pulmonal arteriell hypertensjon (PAH) for å forbedre treningskapasiteten og symptomene. PAH er en patologisk tilstand der trykket i lungearteriene er forhøyet. "Klassen" indikerer alvorlighetsgraden av sykdommen: "klasse III" innebærer en sterk begrensning av fysisk aktivitet. PAH kan være:
- primær (uten identifisert eller familiær årsak);
- forårsaket av sklerodermi (eller progressiv systemisk sklerose, en sykdom preget av unormal vekst av bindevevet som støtter huden og andre organer);
- forårsaket av medfødte hjertefeil (tilstede fra fødselen) med shunts (misdannelser i luftveiene) som forårsaker unormal blodstrøm mellom hjertet og lungene.
- Forbedringer ble også observert hos pasienter med PAH i klasse II. "Klasse II" innebærer en liten begrensning av fysisk aktivitet. Stayveer kan også brukes hos voksne med progressiv systemisk sklerose, der den dårlige blodsirkulasjonen forårsaket av sykdommen har forårsaket "digitale sår" (betennelse i fingrene i hendene) og føtter) Stayveer har som mål å redusere antall nye digitale sår.
Dette legemidlet er det samme som Tracleer, som allerede er autorisert i Den europeiske union (EU). Selskapet som lager Tracleer har avtalt at dets vitenskapelige data kan brukes til Stayveer ("informert samtykke").
Hvordan brukes Stayveer - Bosentan?
Stayveer kan bare fås på resept, og behandlingen bør startes og overvåkes av en lege som har erfaring med behandling av PAH eller progressiv systemisk sklerose. Stayveer er tilgjengelig som tabletter (62,5 mg og 125 mg), som må svelges med vann. Tablettene skal tas om morgenen og om kvelden. Hos voksne er startdosen 62,5 mg to ganger daglig i fire uker, deretter økt til den vanlige dosen på 125 mg to ganger daglig. Hos barn med PAH er dosen som skal brukes basert på kroppsvekt og starter vanligvis med 2 mg per kilo to ganger daglig. For mer informasjon, se pakningsvedlegget. Legen bør vurdere pasientens respons på Stayveer og avgjøre behovet for videre behandling etter åtte uker hos PAH -pasienter som ikke har rapportert forbedring så vel som regelmessig hos progressive systemiske sklerosepasienter med pågående digitale sår. Hvis legen bestemmer seg for å avbryte Stayveer -behandlingen, bør dosen reduseres gradvis. Pasienter som behandles med Stayveer må gis et spesielt notat som oppsummerer hovedinformasjonen om medisinens sikkerhet.
Hvordan fungerer Stayveer - Bosentan?
Det aktive stoffet i Stayveer, bosentan, hemmer et naturlig forekommende hormon som kalles endotelin-1 (ET-1), noe som får blodårene til å trange seg sammen. Derfor forårsaker Stayveer "utvidelse av blodårene. PAH er en svekkende sykdom der alvorlig innsnevring av blodårene i lungene oppstår. Det forårsaker veldig høyt trykk i karene som fører blod fra høyre side av hjertet til lungene. Dette trykket oppstår. Det reduserer mengden oksygen som blodet kan transportere inn i lungene, noe som gjør fysisk aktivitet vanskeligere. Ved å utvide disse blodårene synker blodtrykket og symptomene forbedres. Hos pasienter med progressiv systemisk sklerose og pågående digitale sår forbedrer bosentan blodsirkulasjonen i fingre og tær, og forhindrer utvikling av nye digitale sår.
Hvilken fordel har Stayveer - Bosentan vist under studiene?
I PAH har Stayveer blitt studert i fire hovedstudier: to studier som involverte totalt 245 voksne med PAH klasse III eller IV, primær eller forårsaket av sklerodermi, en studie som involverte 54 voksne med PAH klasse III assosiert med medfødte hjertefeil. som en studie av 185 pasienter med PAH i klasse II. Studiene sammenlignet Stayveer med placebo (et stoff som ikke har noen effekt på kroppen), som begge ble lagt til i standardterapi. Hovedmål for effektivitet var hvor langt pasientene kunne gå på seks minutter (en måte å måle treningskapasitet på) ; Men sykdomsstudien i klasse II så også på endringen i motstand mot blodstrøm i lungekarene (en indikator på fartøyets innsnevring). I PAH klasse III eller IV, primær eller forårsaket av sklerodermi, avslørte de to studiene at pasienter behandlet med Stayveer var i stand til å tilbakelegge større avstander enn pasienter behandlet med placebo etter 16 ukers behandling (44 meter mer i studien større i størrelse); Imidlertid var antallet pasienter med PAH i klasse IV for lite til å støtte bruken av stoffet i denne gruppen. Lignende resultater dukket også opp hos pasienter med medfødte hjertefeil. Hos personer med klasse II PAH induserte Stayveer en reduksjon på 23% i blodet karresistens sammenlignet med placebo etter seks måneders behandling, men avstanden som pasientene kunne gå på seks minutter var lik i de to gruppene. Det ble også utført en studie på 19 barn i alderen 3 til 15 år, der forbedringer i hjerte og arterielle parametere ble observert. Ved progressiv systemisk sklerose med digitale sår, sammenlignet to studier Stayveer med placebo hos totalt 312 voksne. Effektmål ble basert på antall nye digitale sår som hadde utviklet seg i løpet av studier. En av studiene så også på effekten av Stayveer på helbredelsen av 190 pasienter ved å måle tiden det tar for et gitt digitalt sår å helbrede helt hos hver pasient. Stayveer var mer effektiv enn placebo for å redusere dannelsen av nye digitale sår. I den første studien rapporterte pasienter som tok Stayveer i gjennomsnitt 1,4 nye digitale sår etter 16 uker sammenlignet med 2,7 sår hos pasienter som tok placebo. Lignende resultater ble sett i den andre studien etter 24 ukers behandling, men Stayveer hadde ingen effekt på digital sårheling.
Hva er risikoen forbundet med Stayveer - Bosentan?
Hos PAH er de vanligste bivirkningene med Stayveer (som kan påvirke mer enn 1 av 10 personer) hodepine og unormale leverfunksjonstester. Hos pasienter med digitale sår er de vanligste bivirkningene med Stayveer (som kan påvirke mer enn 1 av 10 personer) unormale leverfunksjonstester, ødem og væskeretensjon. Gitt risikoen for å utvikle leverproblemer, vil legen din måle leverenzymnivået ditt før behandling og hver måned under behandling med Stayveer. Den fullstendige listen over bivirkninger rapportert med Stayveer, se pakningsvedlegget Stayveer må ikke brukes til pasienter som har leverproblemer, hos gravide eller fødende kvinner som ikke bruker pålitelige prevensjonsmetoder eller hos kvinner i fertil alder. . pasienter som behandles med ciklosporin A (et legemiddel som virker på immunsystemet). For fullstendig liste over restriksjoner, se pakningsvedlegget.
Hvorfor har Stayveer - Bosentan blitt godkjent?
Byråets komité for medisiner for mennesker (CHMP) bestemte at fordelene til Stayveer er større enn risikoen, og anbefalte at den ble godkjent for bruk i EU.
Hvilke tiltak iverksettes for å sikre sikker og effektiv bruk av Stayveer - Bosentan?
En risikostyringsplan er utviklet for å sikre at Stayveer brukes så trygt som mulig. Basert på denne planen er det lagt til sikkerhetsinformasjon i produktresuméet og pakningsvedlegget for Stayveer, inkludert passende forholdsregler for helsepersonell og pasienter. I tillegg vil selskapet som lager Stayveer, levere et informasjonssett for forskrivere og et informasjonshefte for pasienter i hver medlemsstat for å forklare sikkerheten til Stayveer (spesielt med tanke på virkningen på leveren og graviditeten) og hans interaksjoner. Selskapet forplikter seg også til å nøye overvåke distribusjonen av medisinen i hver medlemsstat og å samle informasjon om bruken til pasienter med progressiv systemisk sklerose med pågående digitale sår.
Lær mer om Stayveer - Bosentan
24. juni 2013 ga EU -kommisjonen en "markedsføringstillatelse" for Stayveer, gyldig i hele EU. For mer informasjon om Stayveer -behandling, les pakningsvedlegget (følger med EPAR) eller kontakt legen din eller apoteket. Siste oppdatering av denne oppsummeringen: 06-2013.
Informasjonen om Stayveer - Bosentan publisert på denne siden kan være utdatert eller ufullstendig. For korrekt bruk av denne informasjonen, se Ansvarsfraskrivelse og nyttig informasjon side.